某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下
图所示的物质之间的变化:
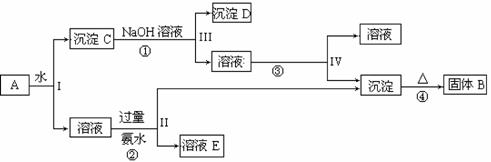 |
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出B、D所含物质的化学式。固体B ;
沉淀D 。
(3)试剂③是 (填化学式)
(4)写出①的化学反应方程式 ;
②的离子反应方程式 。
配制物质的量浓度为0.2 mol/L的NaOH溶液500 mL,填空并请回答下列问题:
(1)填写①②对应的问题
| 应称量NaOH的质量/g | 已给仪器 | 除已给仪器外还需要的玻璃仪器 |
| ① | 烧杯、量筒、胶头滴管、500 mL容量瓶 | ② |
(2)下列操作中,容量瓶所具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.用来加热溶解固体溶质
(3)下列操作对配制的NaOH溶液浓度有偏高影响的是________。
A.称量NaOH固体时,露置在空气的时间过长
B.选用的容量瓶内有少量的蒸馏水
C.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
D.在定容时仰视容量瓶刻度线
将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加
入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所
示。则下列说法不正确的是
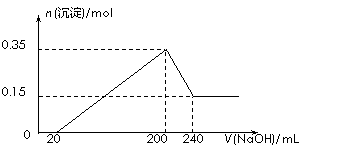 |
A.镁和铝的总质量为9 g
B.最初20 mLNaOH溶液用于中和过量的硫酸
C.硫酸的物质的量浓度为2.5 mol·L–1
D.生成的氢气在标准状况下的体积为11.2 L
 A B C D
A B C D