[化学——有机化学基础]
|
(1)氢化阿托醛被氧化后的含氧官能团的名称是 ;
(2)在合成路线上②③的反应类型分别为② ③ 。
(3)反应④发生的条件是 ;
(4)反应⑤的化学方程式为 ;
(5)D有多种同分异构体,能满足苯环上有两个取代基,且能使FeCl3溶液显紫色的同分异构体有 种。
[化学——化学与技术]
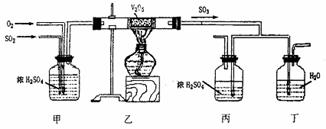
下面的装置是仿照工业上制备硫酸的工艺流程设计出来的,用于探究工业上为何采用98.3%的浓硫酸吸收三氧化硫。
|
请回答下列问题:
(1)写出沸腾炉内煅烧黄铁矿的化学方程式 ;
(2)上图中的乙、丙分别相当于工业上制取硫酸设备中的 、 ;
(3)丁中的现象为 ;
(4)下图是压强对SO2平衡转化率的影响:
|
温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
对SO2转化为SO3的反应,增大压强可使转化率 ,工业生产中通常采用压操作的原因是 。
硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种,某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式,实验用到的仪器如下图所示:
|
[提出猜想]
Ⅰ.所得气体的成分可能只含 一种;
Ⅱ.所得气体的成分可能含有 二种;
Ⅲ.所得气体的成分可能含有SO2、SO3、O2三种。
[实验探究]
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。
请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
(填序号);
(2)若实验结束,B中量筒没有收集到水,则证明猜想 正确;
(3)实验过程,仪器C的作用是 ;
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4 的质量/g | 仪器C增 加的质量/g | 量筒中水的体积折算成标 准状况下气体的体积/mL |
| ① | 6.4 | 2.88 | 224 |
| ② | 6.4 | 2.56 | 448 |
请通过计算,推断出第①小组和第②小组的实验条件下CuSO4分解的化学反应方程式:
①组 ;
②组 。
研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义。
(1)下列措施中,有利于降低大气中的CO2、SO2、NO2浓度的有 (填字母);
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)为开发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料。写出由CO和H2生产甲醇的化学方程式 ,用该反应合成1mol液态甲醇吸收热量131.9kJ。又知![]()
![]() 。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式
。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式
;
|
根据图示回答下列问题:
①![]()
![]() 2SO3(g)的
2SO3(g)的
△H 0(填“>”或“<”);
②若温度T1、T2时,反应的化学平衡常数分别
为K1、K2,则K1 K2;若反应进行到
状态D时, (填“>”、“<”或“=”)

 转化率/% 压强/MPa
转化率/% 压强/MPa
