题目内容
[化学——化学与技术]
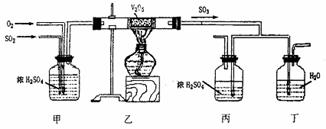
下面的装置是仿照工业上制备硫酸的工艺流程设计出来的,用于探究工业上为何采用98.3%的浓硫酸吸收三氧化硫。
|
请回答下列问题:
(1)写出沸腾炉内煅烧黄铁矿的化学方程式 ;
(2)上图中的乙、丙分别相当于工业上制取硫酸设备中的 、 ;
(3)丁中的现象为 ;
(4)下图是压强对SO2平衡转化率的影响:
|
温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
对SO2转化为SO3的反应,增大压强可使转化率 ,工业生产中通常采用压操作的原因是 。
[化学与技术]
(1)4FeS2+11O2 2Fe2O3+8SO2(2分)
(2)转化器 吸收塔(各1分,共2分)
(3)有酸雾(或有白雾)(1分)
(4)增大(1分) 常压SO2的转化率已很大(2分)

练习册系列答案
相关题目
【化学-化学与技术】某强酸性工业废水中含有Fe2+、Fe3+、Cu2+,设计实验方案用沉淀法除去铁离子,得到较纯的Cu2+溶液.有关氢氧化物沉淀的pH如下表:
(1)从表中数据分析,为什么不能直接加NaOH将溶液pH调到9.7来除去Fe3+和Fe2+ .
(2)实际应用中则是先加一定量的次氯酸钠,然后再调节溶液pH.次氯酸钠的作用是 .
(3)pH应调节到什么范围 ,为什么 .
(4)调节pH适宜的试剂是
A.氢氧化钡B.碳酸镁,C、氧化铜、D、稀盐酸
理由 .
| 金属离子 | pH | |
| 开始沉淀 | 沉淀完全 | |
| Fe2+ | 6.3 | 9.7 |
| Cu2+ | 4.7 | 6.7 |
| Fe3+ | 1.9 | 3.2 |
(2)实际应用中则是先加一定量的次氯酸钠,然后再调节溶液pH.次氯酸钠的作用是
(3)pH应调节到什么范围
(4)调节pH适宜的试剂是
A.氢氧化钡B.碳酸镁,C、氧化铜、D、稀盐酸
理由
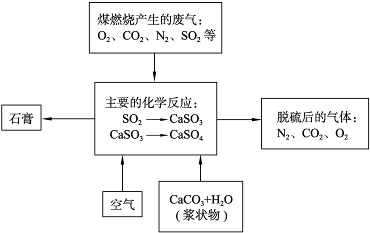
【化学--化学与技术】
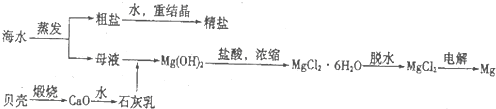
海洋是一座巨大的宝藏,海洋资源的开发与利用具有广阔的前景.某地海水的pH在7.5~8.6之间,其中主要离子的含量如下表:
(1)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图1.其中阴 (阳)离子交换膜只允许阴(阳)离子通过.
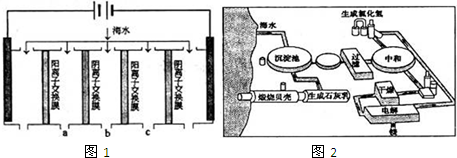
①阴极的电极反应式为 .
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式 .
③淡水的出口为a、b、c中的 出口.
(2)如图2是工业上生产镁的流程.
①干燥步骤中将氯化镁的水合晶体转化为无水氯化镁的操作方法是 .
②整个生产流程中,循环使用的物质是 .
③有人认为:过滤步骤后,直接加热Mg(OH)2得MgO,再电解熔融的MgO制金属镁,这样可优化生产过程.你的观点是 (填“同意”或“不同意”);理由是 .
海洋是一座巨大的宝藏,海洋资源的开发与利用具有广阔的前景.某地海水的pH在7.5~8.6之间,其中主要离子的含量如下表:
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO 42- | HCO 3+ | 含量/mg?L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |

①阴极的电极反应式为
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式
③淡水的出口为a、b、c中的
(2)如图2是工业上生产镁的流程.
①干燥步骤中将氯化镁的水合晶体转化为无水氯化镁的操作方法是
②整个生产流程中,循环使用的物质是
③有人认为:过滤步骤后,直接加热Mg(OH)2得MgO,再电解熔融的MgO制金属镁,这样可优化生产过程.你的观点是
 转化率/% 压强/MPa
转化率/% 压强/MPa