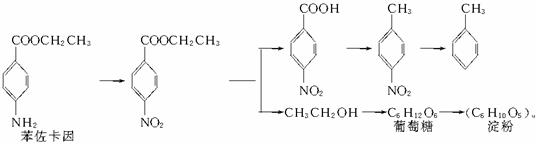
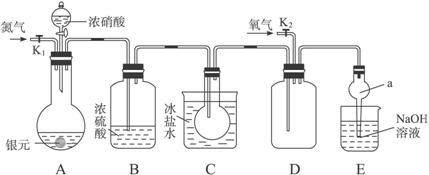
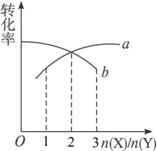
1932年美国化学家鲍林(Linns Pauling)首先提出了电负性的概念。电负性(用x表示)也是元素的一种重要性质,不同元素的原子在分子内吸引电子的能力大小可用x来表示,若x越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方。下表给出的是原子序数小于20的16种元素的电负性数值:
0 31684 31692 31698 31702 31708 31710 31714 31720 31722 31728 31734 31738 31740 31744 31750 31752 31758 31762 31764 31768 31770 31774 31776 31778 31779 31780 31782 31783 31784 31786 31788 31792 31794 31798 31800 31804 31810 31812 31818 31822 31824 31828 31834 31840 31842 31848 31852 31854 31860 31864 31870 31878 203614
元素 | H | Li | Be | B | C | N | O | F |
电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
元素 | Na | Mg | Al | Si | P | S | Cl | K |
电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
请仔细分析,试完成下列有关问题:
(1)根据表中所给数据分析推测:
同主族的不同元素的x值变化的规律是:____________________________________________;
x值与原子半径的关系是:________________________________________________________。
(2)预测周期表中电负性最大的元素应为_______(填元素符号);估计钙元素的电负性的取值范围:__________<x<__________。
(3)预测周期表中,x值最小的元素位于第_________周期_________族。(放射性元素除外)
(4)经验规律告诉我们:当成键的两原子相应元素的x差值Δx>1.7时,一般形成的键为离子键,当Δx<1.7时,一般形成的键为共价键。试推断AlBr3中化学键的类型为__________,其理由是__________________________________________________。
 ?
?