①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2—3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50 ℃—80 ℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2—3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。
请完成下列问题:
(1)实验步骤①的目的是_________________,加热的作用是__________________________。
(2)实验步骤②明显不合理,理由是______________________________________________。
(3)实验步骤④中用少量冰水洗涤晶体,其目的是_________________;_________________。
(4)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4·7H2O、FeSO4·4H2O和FeSO4·H2O。硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在56.7 ℃、64 ℃温度下可同时析出两种晶体)。
硫酸亚铁的溶解度和析出晶体的组成
温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||
请根据表中数据作出硫酸亚铁的溶解度曲线。

(5)若需从硫酸亚铁溶液中结晶出FeSO4·4H2O,应控制的结晶温度(t)的范围为_________________。
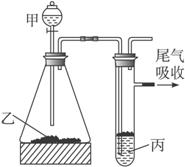
| 甲 | 乙 | 丙 | 结论 |
A | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
B | 盐酸 | 硫化亚铁 | 溴水 | 还原性:C->Br->S2- |
C | 浓盐酸 | 高锰酸钾 | 溴化钾溶液 | 氧化性:浓盐酸>Cl2>Br2 |
D | 水 | 电石 | 溴水 | 稳定性:H2O>C2H2>Br2 |


