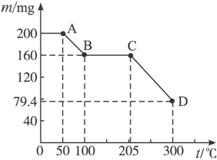
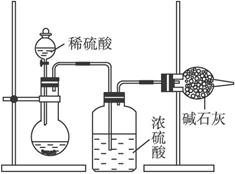
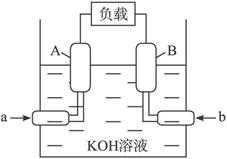
方法一:将尾气通入氨水,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。已知(NH4)2SO4和NH4HSO4的分解温度均高于200 ℃,欲测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液50.00 mL,加热至120 ℃左右,使氨气全部逸出,测得有关实验数据以下:
实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L(标准状况) |
① | 7.24 | 50.0 | 1.792 |
② | 14.48 | 50.00 | 3.584 |
③ | 21.72 | 50.00 | 4.032 |
④ | 28.96 | 50.00 | 3.136 |
(1)若取3.62 g样品用同种方法实验时,生成氨气的体积(标准状况)为__________L。
(2)该混合物中(NH4)2SO4和NH4HSO4的物质的量之比为__________。
(3)求所用NaOH溶液的物质的量浓度(写出计算过程)。
方法二:用NaOH溶液、石灰及O2吸收尾气SO2,以制取石膏(CaSO4·2H2O),此过程的中间产物是NaHSO3。实际操作中以调节尾气排放的流量来取得SO2与NaOH间物质的量的最佳比值,从而提高亚硫酸氢钠的产量。试写出n(SO2)/n(NaOH)在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)的关系式,填入下表:
n(SO2)/n(NaOH) | n(NaHSO3) |
|
|
|
|
|
|
|
|
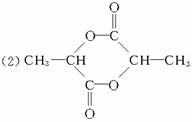
(1)烯烃的复分解反应就是两种烯烃交换双键两端的基团,生成两种新烯烃的反应。请写出在催化剂作用下,两个丙烯分子间发生复分解反应的化学方程式_________________。
(2)烯烃与高锰酸钾酸性溶液反应的氧化产物有如下的对应关系:
烯烃被氧化的部位 | =CH2 | RCH= |
|
氧化产物 | CO2 | R—COOH |
|
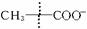
已知某烯烃的分子式为C5H10,它与高锰酸钾酸性溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是_________;若为二氧化碳和丁酮(![]() ),则此烯烃的结构简式是_____________________。
),则此烯烃的结构简式是_____________________。
A.附着于试管内壁的苯酚,可用碱液洗涤
B.用结晶法可以除去硝酸钾中混有的少量氯化钠
C.切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割
D.实验时,不慎打翻燃着的酒精灯,可立即用湿抹布盖灭火焰
E.浓硫酸不小心沾到皮肤上,立刻用稀烧碱溶液洗涤
F.在氢氧化铁胶体中滴加少量稀硫酸会产生沉淀
(2)下表是某种常见金属的部分性质:
颜色状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
银白色固体 | 较软 | 2.70 g·cm-3 | 660.4 ℃ | 良好 | 良好 | 良好 |
将该金属投入冷水中无变化,投入稀盐酸中可产生大量的无色气体。试回答:
①推断该金属可能的一种用途__________,该金属的活动性比铜__________(填“强”或“弱”)。
②请自选试剂,设计不同的实验探究该金属与铁的活动性强弱,并完成下表:
猜想 | 验证方法 | 预测实验现象 |
该金属比铁活泼 |
|
|
该金属活泼性比铁弱 |
|
|