不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。
0 30740 30748 30754 30758 30764 30766 30770 30776 30778 30784 30790 30794 30796 30800 30806 30808 30814 30818 30820 30824 30826 30830 30832 30834 30835 30836 30838 30839 30840 30842 30844 30848 30850 30854 30856 30860 30866 30868 30874 30878 30880 30884 30890 30896 30898 30904 30908 30910 30916 30920 30926 30934 203614
下面是某些短周期元素的x值:
元素符号 | Li | Be | B | C | O | F |
x值 | 0.98 | 1.57 | 2.04 | 2.25 | 3.44 | 3.98 |
元素符号 | Na | Al | Si | P | S | Cl |
x值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值变化规律,确定Mg、N的x值范围:________<x(Mg)<________,________<x(N)<________。
(2)推测x值与原子半径关系是________,根据短周期元素的x值变化特点,体现了元素性质的________变化规律。
(3)某有机化合物结构式为:
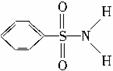 ,其中S—N键中你认为共用电子对偏向谁?________(写原子名称)。
,其中S—N键中你认为共用电子对偏向谁?________(写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的x差值(Δx)即x>1.7时,一般为离子键;当Δx<1.7时,一般为共价键。试推断AlBr3中化学键类型是________。
(5)预测元素周期表中,x值最小的元素的位置:_______(放射性元素除外)。