(08上海建平中学期末)某同学用下列装置制备并检验Cl2的性质。
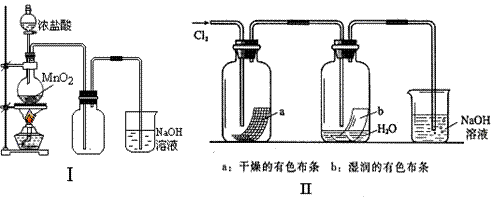 |
(1)II图中褪色的是 (填a或b),烧杯中反应的离子方程式是
(2)①将Cu丝换成Fe丝,做III实验,结果也能点燃,你认为Fe丝也可点燃的理由是 。
a.Fe与Cu都是金属元素 b.Fe的熔点比Cu高
c.Fe的密度比Cu小 d.Fe的金属性比Cu强

②通常由燃烧产物(FeCl3)配制其溶液的方法 。
(3)将IV装置放置在光亮的地方(日光没有直接照射),一会儿后,观察到量筒壁上有油状
液滴生成,饱和食盐水中有少量固体析出,量筒内黄绿色气体颜色变浅 ,量筒内液面上升等。
1油状液滴的成分可能是(写分子式) ,
2水槽用饱和食盐水而不用水的原因是_____________ ____________________。
3饱和食盐水中有少量固体析出,其原因是_______________ ______________。
(4)将硫酸溶液滴入II图烧杯中,至溶液显酸性,结果也有Cl2生成,该反应的离子方程
式是 。
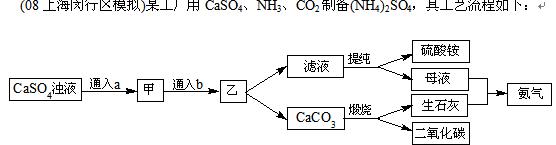
(08上海松江区模拟)过碳酸钠是由碳酸钠和过氧化氢复合形成的一种新型氧系漂白剂,具有碳酸钠和过氧化氢的双重性质,其分子式为2Na2CO3?3H2O2,已知过渡元素的金属离子可作为催化剂使之分解。
它的制备原理和湿法生产路线如下:2Na2CO3 + 3H2O2 → 2 Na2CO3?3H2O2
 |
回答下列问题:
(1)反应控制在0~5℃条件下进行,其主要原因是 ,流程中的“分离”指的是实验操作中的 ;
(2)工业碳酸钠中一般含有少量锰、铜等金属离子(用M2+表示),加入稳定剂的作用是将M2+沉淀而除去,M2+对产品的不良影响是 ,
若加入的稳定剂是Na2SiO3,反应的离子方程式为 ;
(3)加入的食盐为盐析剂,其原理是降低过碳酸钠的溶解度使之析出。盐析是物理变化还是化学变化? ;
(4)过碳酸钠在生产上的应用是利用它分解所释放的H2O2。以铜为原料用H2O2氧化是工业上制胆矾的方法之一。做法是:
将铜丝放到一定量的稀硫酸中,控温在50℃,加入一定量的H2O2溶液,反应0.5h后,升温到60℃,再持续反应1 h,过滤后取滤液,再经过“某些操作”、减压抽滤,用少量95%的酒精淋洗后晾干,可得CuSO4?5H2O。
①在反应中,起氧化作用的是H2O2,写出H2O2在稀硫酸中氧化单质铜的化学反应方程式 ;
②处理滤液时的“某些操作”指的是 ;
③晶体采用酒精淋洗的优点是 。


 (08上海松江区模拟)乙酸乙酯是重要的工业原料和溶剂。现利用如图
(08上海松江区模拟)乙酸乙酯是重要的工业原料和溶剂。现利用如图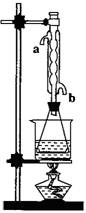 ⑶对于制乙酸乙酯的上述装置,为了提高产率,请提出
⑶对于制乙酸乙酯的上述装置,为了提高产率,请提出