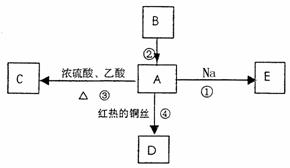
有如下规律可判断元素原子的失电子能力:比较元素的单质与水(或非氧化性酸)反应置换出氢气的难易程度。置换反应越容易发生,元素原子失电子能力越强。某化学活动小组为了验证上述规律设计了以下实验进行探究,请你填写下表有关内容:
| 实验内容 | 实验现象 | 实验结论 |
|
| 同一周期自左而右元素原子失电子的能力逐渐 ;同一主族自上而下元素原子失电子能力依次 。 | |
|
|
某课外实验小组利用稀硫酸与金属铁反应探究影响化学反应速率的因素,得到如下实验数据:
![]()
| 实验
| 铁的
| 铁的
| c/(H2SO4)
| V(H2SO4)
| 溶液温度/℃ | 金属消失
| |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 铁片 | 0.7 | 50 | 20 | 36 | 250 |
| 2 | 0.10 | 铁片 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 铁粉 | 0.8 | 50 | 20 | 36 | 25 |
| 4 | 0.10 | 铁片 | 1.0 | 50 | 20 | 35 | 125 |
| 5 | 0.10 | 铁片 | 1.0 | 50 | 35 | 50 | 50 |
![]() 分析上述数据,回答下列问题:
分析上述数据,回答下列问题:
![]() (1)实验2和3表明, 对反应速率有影响,影响规律是
(1)实验2和3表明, 对反应速率有影响,影响规律是
![]() ;
;
![]() (2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号);
![]() (3)本实验中影响反应速率的其他因素还有 ,能体现该影响因素的实验序号是 ;
(3)本实验中影响反应速率的其他因素还有 ,能体现该影响因素的实验序号是 ;
![]() (4)在实验4中滴入几滴硫酸铜溶液,金属消失的时间小于125s。
(4)在实验4中滴入几滴硫酸铜溶液,金属消失的时间小于125s。
![]() 原因是
原因是
![]() ;
;
![]() (5)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,试从反应过程能量的变化角度推测其原因
(5)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,试从反应过程能量的变化角度推测其原因
![]() 。
。