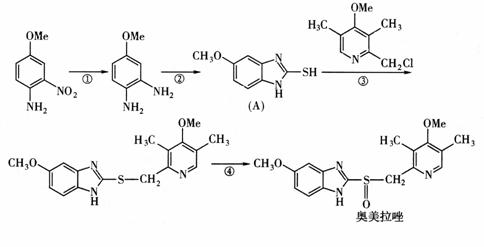
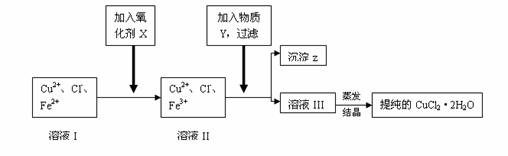
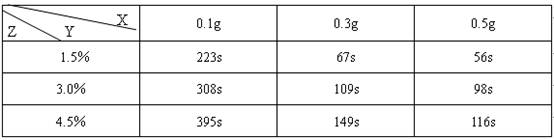
Al和Si、Ge和As在元素周期表金属和非金属过渡位置上,在其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。请回答下列问题:
(1)As的价层电子构型为
(2)AlCl3 是化工生产中的常用催化剂,熔点为192.6℃,熔融状态以二聚体Al2Cl6形式存在,其中铝原子与氯原子的成键类型是
(3)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,AlN晶体与金刚石类似,每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。在四大晶体类型中,AlN属于 晶体。
(4)Si和C同主族,Si、C和O成键情况如下:
| C―O | C=O | Si―O | Si=O | |
| 键能/kJ?mol―1 | 360 | 803 | 464 | 640 |
在C和O之间可以形成双键形成CO2分子,而Si和O则不能和碳那样形成有限分子原因是
。
(5)SiCl4(l)常用作烟雾剂,原因Si存在3d轨道,能同H2O(l)配位而剧烈水解,再潮湿的空气中发烟,试用化学方程式表示其原理
与化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示,K只与温度有关)。下表是几种常见弱酸的电离平衡常数(25℃)。
| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH | 1.76×10-5 |
| H2CO3 | H2CO3 HCO3― | K1==4.31×10-7 K2==5.61×10-11 |
| H3PO4 | H3PO4 H2PO4 HPO42 | K1==7.1×10-3 K2==6.3×10-8 K3==4.2×10-13 |
回答下列各题:
(1)温度升高时, (填“促进”或“抑制”)弱酸的电离,K值 (填“增大”、“减小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱关系是
。
(3)若把CH3COOH、H2CO3、HCO3-、H3PO4、H2PO4、HPO42-都看作是酸,则它们酸性强弱顺序是_________________________________________。
(4)若醋酸的起始浓度为0.010mol/L,则平衡时溶液的pH是多少?(写出计算过程,结果以对数形式表示)