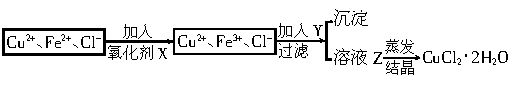题目内容
制取纯净CuCl2?2H2O的生产过程是:
(1)用粗CuO(含少量铁)溶解在足量的稀盐酸里加热、过滤,得到CuCl2(含FeCl2)的溶液,经测定,溶液的PH值为3。
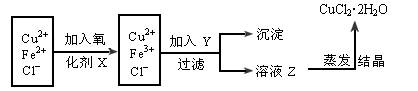
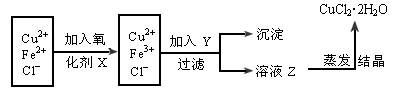
(2)对(1)的溶液按下列步骤进行提纯:
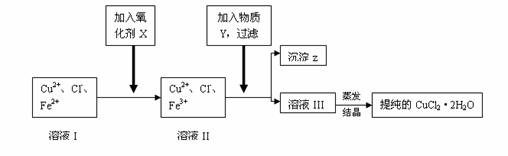
![]() 已知:①可做氧化剂的物质有(A)KMnO4 (B)K2Cr2O7 (C)H2O2 (D)NaClO
已知:①可做氧化剂的物质有(A)KMnO4 (B)K2Cr2O7 (C)H2O2 (D)NaClO
②Cu2+ 、Fe2+在PH值为4~5时不水解,而Fe3+却几乎全部水解。
试回答:
(1)加入的氧化剂X是(答编号): ;
加入X的作用是: ;
反应的离子方程式是: 。
(2)物质Y是 ;沉淀Z是 。加入Y能形成沉淀Z的原因是: 。
(3)分离出沉淀Z,并将溶液III蒸发欲获得晶体CuCl2?2H2O。采取什么措施才能顺利得到晶体CuCl2?2H2O?______________________ 。
(1)C;把Fe2+ 氧化成Fe3+;2Fe2++H2O2+2H+=2Fe3++2H2O
(2)CuO或Cu(OH)2或CuCO3;Fe(OH)3(若有Y也不扣分);CuO与H+反应,使溶液的PH值升高,促进了Fe3+的水解,当PH值为4~5时,Fe3+几乎完全水解生成
Fe(OH)3。
(3)用HCl气体做保护气,防止CuCl2水解。

练习册系列答案
相关题目