同一主族的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性强弱是H3XO4<H3YO4<H3ZO4,下列推断正确的是( )
| A、原子序数:X<Y<Z | B、元素的非金属性强弱:X>Y>Z | C、气态氢化物稳定性:XH3<YH3<ZH3 | D、电子层数:X>Y>Z |
下列有关化学用语表述正确的是( )
A、CO2的比例模型: | B、铝离子的结构示意图: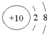 | C、乙烯的结构简式 CH2CH2 | D、甲基的电子式: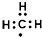 |
下列化学用语错误的是( )
A、氯化氢分子的电子式: | B、乙烯的结构简式:CH2=CH2 | C、乙酸中的官能团:-COOH | D、氯的原子结构示意图: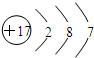 |
下列有关表达不正确的是( )
A、具有16个质子、16个中子和18个电子的微粒是
| ||
B、NH3的形成过程为: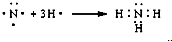 | ||
| C、HCN的结构式为:H-C≡N | ||
| D、有机还原剂LiAlH4中,氢显-1价 |
23He 可以作为核聚变材料,下列关于23He的叙述正确的是( )
| A、23He和13H互为同位素 | B、23He原子核内中子数为2 | C、23He代表有2个质子和3个中子的氦原子 | D、23He原子核外电子数为2 |
有关化学键和晶体的说法中正确的是( )
| A、离子键的本质是静电作用,阴阳离子电荷越大、离子半径越小,静电作用越强 | B、共价键的本质是共用电子对,因此必须由成键的两原子各提供一个电子形成 | C、分子晶体的基本微粒是分子,分子晶体熔沸点由分子内部共价键强弱决定 | D、原子晶体由于是空间网状结构,因此只能由碳、硅两元素构成 |
在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境分析指示物.下列说法正确的是( )
| A、34S原子核内中子数为16 | B、16O2比18O2沸点更低 | C、2H+的酸性比1H+的酸性更强 | D、13C和15N原子核内的质子数相差2 |
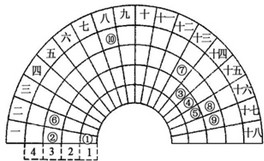 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A、②、⑧、⑨对应简单离子半径依次减小 | B、⑥的氯化物的熔点比⑦的氯化物熔点低 | C、元素⑩处于常见周期表第四周期第VⅢB族 | D、①分别与③、④、⑤均可形成既含极性键又含非极性键的化合物 |
下列化学用语表述正确的是( )
A、S2-的结构示意图: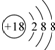 | B、氮原子的轨道表示式: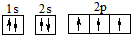 | C、CO2的比例模型: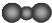 | D、氨气分子的结构式: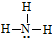 |
符号
Cl中左上角的“35”代表( )
35 17 |
| A、元素的质量数 |
| B、原子的质量数 |
| C、元素的平均相对原子质量 |
| D、元素的近似相对原子质量 |