关于化学键的各种叙述正确的是( )
| A、在离子化合物里,只存在离子键,没有共价键 | B、只有共价键形成的物质,不一定是共价化合物 | C、非极性键只存在于双原子的单质分子中 | D、由不同元素组成的多原子分子里,一定只存在极性键 |
有关四氯化碳的化学用语正确的是( )
A、结构简式: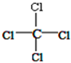 | B、电子式: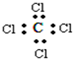 | C、结构简式:CCl4 | D、比例模型: |
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子.下列有关这些元素性质的说法一定正确的是( )
| A、X元素的氢化物的水溶液显碱性 | B、Z元素的离子半径大于W元素的离子半径 | C、Z元素的单质在一定条件下能与X元素的单质反应 | D、Y元素最高价氧化物的晶体具有很高的熔点和沸点 |
在一定条件下,某容器中充入N2和H2合成NH3,以下叙述错误的是( )
| A、开始反应时,正反应速率最大,逆反应速率为零 | B、随着反应的进行,正反应速率逐渐减小,最后减小为零 | C、随着反应的进行逆反应速率逐渐增大,后保持恒定 | D、随着反应的进行,正反应速率逐渐减小,最后与逆反应速率相等且都保持恒定 |
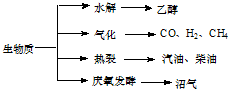 秸秆、稻草等生物质是一种污染小的可再生能源,其主要转化途径及主要产物如图.下列有关说法错误的是( )
秸秆、稻草等生物质是一种污染小的可再生能源,其主要转化途径及主要产物如图.下列有关说法错误的是( )| A、生物质能所含能量本质上来源于太阳能 | B、由秸秆等物质水解获得的乙醇属生物质能 | C、生物质裂解获得的汽油、柴油等属于纯净物 | D、由秸杆稻草等发酵获得的沼气,主要成分是甲烷 |
下列图示与对应的叙述相符的是( )

| A、图1曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,P点时二者恰好反应完全且溶液呈中性 | B、图2表示H2(g)与O2(g)反应生成H2O(l)或H2O(g)时的能量变化的关系 | C、图3表示向Ba(HCO3)2溶液中滴入NaOH溶液时所得沉淀质量的变化 | D、由图4表示的反应速率随温度变化的关系可知该反应的△H>0 |
已知25℃时:①NH4+(aq)+OH-(aq)=NH3?H2O(aq)△H=a kJ?mol-1
②NH4+(aq)+H2O(l)?NH3?H2O(aq)+H+(aq)△H=bkJ?mol-1
向20mL0.1mol/L氨水中逐滴加入0.1mol/L盐酸,下列有关说法正确的是( )
②NH4+(aq)+H2O(l)?NH3?H2O(aq)+H+(aq)△H=bkJ?mol-1
向20mL0.1mol/L氨水中逐滴加入0.1mol/L盐酸,下列有关说法正确的是( )
| A、水电离过程的热化学方程式可表示为:H2O(l)?H+(aq)+OH-(aq)△H=(a-b)KJ/mol | B、当滴入10mL盐酸时,溶液中:c(NH4+)+c(NH3?H2O)=2c(Cl-) | C、随着盐酸的逐滴加入,水电离的c(OH-)总是逐渐减小 | D、当滴入20 mL盐酸时,溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
已知乙炔与苯蒸气完全燃烧的热化学方程式如下所示:
①2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)△H=-2 600kJ/mol
②2C6H6(g)+15O2(g)→12CO2(g)+6H2O(l)△H=-6 590kJ/mol,下列说法正确的是( )
①2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l)△H=-2 600kJ/mol
②2C6H6(g)+15O2(g)→12CO2(g)+6H2O(l)△H=-6 590kJ/mol,下列说法正确的是( )
| A、2 mol C2H2(g)完全燃烧生成气态水时放热大于2 600 kJ | B、2 mol C6H6(l)完全燃烧生成液态水时放热大于6 590 kJ | C、3分子C2H2(g)化合生成C6H6(g)的过程属于放热反应 | D、相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多 |