下列说法错误的是( )
| A、化学可以识别、改变和创造分子 | B、在化学反应中,反应前后电子总数可能发生变化 | C、摩尔是一个单位,用于计量物质所含微观粒子的多少 | D、在化学反应中,反应前后原子种类、原子数目和质量一定不变 |
下列有关热化学方程式及其叙述正确的是( )
| A、氢气的燃烧热为285.5kJ/mo1,则水电解的热化学方程式为:2H2O(l)═2H2(g)+O2(g);△H=+285.5kJ/mol | ||||
B、1mol甲烷完全燃烧生成CO2和H2O(l)时放出890kJ热量,它的热化学方程式为
| ||||
| C、已知2C(s)+O2(g)═2CO(g);△H=-221kJ?mol-1,则C的燃烧热为110.5kJ/mol | ||||
| D、HF与NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ/mol |
 能源是现代社会发展的支柱之一.
能源是现代社会发展的支柱之一.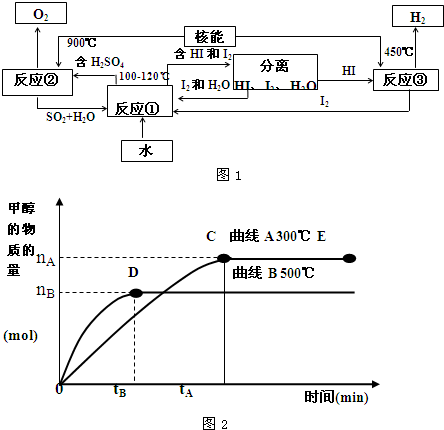
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
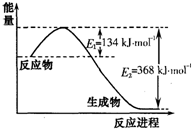
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题: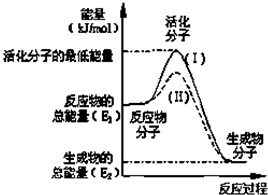 在化学反应中,只有活化分子才能发生有效碰撞而发生化学反应.使普通分子变成活化分子所需提供的平均能量叫活化能,其单位通常用kJ?mol-1表示.请观察如图,回答下列问题:
在化学反应中,只有活化分子才能发生有效碰撞而发生化学反应.使普通分子变成活化分子所需提供的平均能量叫活化能,其单位通常用kJ?mol-1表示.请观察如图,回答下列问题: 二甲基亚砜
二甲基亚砜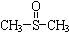 有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜(
有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜( ),有关反应如下:
),有关反应如下: