少量的CO2通入到下列溶液中,有沉淀生成的是( )
| A、石灰水 | B、CaCl2溶液 | C、Ba(NO3)2溶液 | D、Ca(HCO3)2溶液 |
在化学学习与研究中用类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否.下列类推结论中正确的是( )
| A、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O | B、CO2和SiO2的化学式相似,则CO2与SiO2的物理性质也相似 | C、CO2不能与CaCl2溶液反应,则SO2也不能与CaCl2溶液反应 | D、Na2O中阳、阴离子的个数之比为2:1,可推出Na2O2中阳、阴离子的个数之比为1:1 |
下列说法违背化学原理的是( )
| A、SO2的催化氧化是一个放热的反应,升高温度,反应速率加快 | B、“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量较高 | C、A(g)+3B(g)?2C(g)达平衡后,恒温,增压,平衡正向移动,平衡常数K值增大 | D、在KI溶液中加入氯化银固体,沉淀变成黄色,说明同温度下Ksp(AgI)<Ksp(AgCl) |
下列工业生产所用主要原料(括号内物资)不合理的是( )
| A、合成NH3(焦碳、空气、水) | B、炼铁(铁矿石、焦碳、石灰石、空气) | C、生产乙烯(酒精、浓硫酸) | D、水泥工业(石灰石、粘土) |
下列关于工业生产说法错误的是( )
| A、在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳 | B、在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 | C、在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室 | D、工业上采用电解熔融氯化铝的方法制取金属铝 |
生产、生活中的有些现象看上去很相近,但原理相差甚远.下列现象中产生原理相同的是( )
| A、在两只烧杯中分别放置干冰和浓硝酸,都有白雾产生 | B、碘和锌在少量水作用下剧烈反应,钠在氯气中燃烧,都有烟产生 | C、铁酸钾(K2FeO4)和氯化亚铁与氯水的混合物,都可用于自来水消毒及净化 | D、在空气中亚硫酸钠与偏铝酸钠都会变质 |
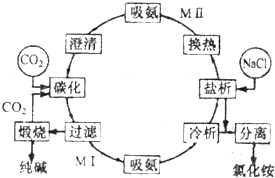 侯氏制碱法流程如图所示,有关说法不正确的是( )
侯氏制碱法流程如图所示,有关说法不正确的是( )| A、该工艺中原料是食盐、氨、二氧化碳及水,最终产品是纯碱和氯化铵 | B、工艺中M I处吸氨与MⅡ处的目的完全相同 | C、该工艺中CO2再利用,可以减少温室气排放 | D、该过程中涉及的主要反应有:NH3+H2O+CO2=NH4HCO3 NH4HCO3+NaCl=NH4Cl+NaHCO32NaHCO3═Na2CO3+H2O+CO2 |
下列根据有关原理或规律得出的推断合理的是( )
| A、根据酸性氧化物的性质,推知有反应:SiO2+H2O=H2SiO3 | ||
B、根据强电解质的电离原理,推知1mol?L-1NaHSO4溶液中HSO
| ||
| C、根据盖斯定律,推知在相冋条件下,红磷或白磷燃烧生成1molP2O5回体时,放出的热量相等 | ||
| D、根据同主族物质性质的相似性和递变性,推知CsOH属于强碱 |
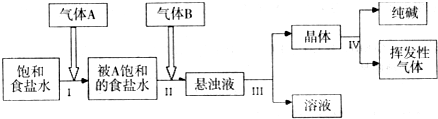
侯氏制碱法原理是:将NH3和CO2气体通入饱和食盐水中即可获得NaHCO3和NH4Cl 的混合物,然后分离出 NaHCO3 再加热制得纯碱.其流程如下:
参照下表:
回答下列问题:
(l)气体A、B依次是
A、CO2,NH3 B、NH3,CO2 C、任何顺序都可以
(2)写出(Ⅰ)和(Ⅱ)步骤总的化学反应方程式: 由反应原理可知,a 9.6(填“<”、“>”或“=“)
(3)操作(Ⅲ)的名称是: ,化学实验室进行该操作用到的玻璃仪器有: .
(4)经步骤(Ⅲ)所得液体中含有的盐为(写化学式): 经过 (填操作名称)后可以得到化肥.
(5)每当通入NH344.8L(已折合成标准状况下)时可以得到纯碱100.0g,则NH3的利用率为 .
0 22303 22311 22317 22321 22327 22329 22333 22339 22341 22347 22353 22357 22359 22363 22369 22371 22377 22381 22383 22387 22389 22393 22395 22397 22398 22399 22401 22402 22403 22405 22407 22411 22413 22417 22419 22423 22429 22431 22437 22441 22443 22447 22453 22459 22461 22467 22471 22473 22479 22483 22489 22497 203614

参照下表:
| 物质 | CO2 | NH3 | NaHCO3 | NH4Cl | NaCl |
| 溶解度(20℃) | V水:V二氧化碳=1:1 | V水:V氯气=1:700 | 9.6g | 37.2g | ag |
(l)气体A、B依次是
A、CO2,NH3 B、NH3,CO2 C、任何顺序都可以
(2)写出(Ⅰ)和(Ⅱ)步骤总的化学反应方程式:
(3)操作(Ⅲ)的名称是:
(4)经步骤(Ⅲ)所得液体中含有的盐为(写化学式):
(5)每当通入NH344.8L(已折合成标准状况下)时可以得到纯碱100.0g,则NH3的利用率为
 如图所示表示氢气和氯气反应的示意图,试回答:
如图所示表示氢气和氯气反应的示意图,试回答: