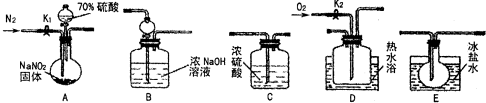
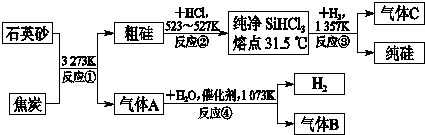
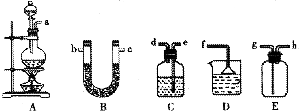
氮及其化合物与我们的吃、穿、住、行、健康等都有着密切的联系,也是高中化学学习中重要的一部分.请回答下列问题:
(1)一定条件下,向一个2L的密闭容器中充入2molN2和6molH2,反应达平衡时放出93kJ热量,生成NH3的浓度为1mol/L,试写出该反应的热化学方程式 .
(2)现有一支l0mL的试管,充满NO倒置于水槽中,向试管中缓缓通A-定量氧气,当试管内液面稳定时,剩余气体2mL.则通入氧气的体积可能为 .
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2g)?4NO(g)+6H2O(g).
①恒温恒容下,平衡时NH3的转化率甲 乙.(填“>”、“、”或“<”)
②恒温恒容下,若要使丙与甲平衡时各组分浓度相同,则x= ,y= ,z= .
(4)向容积相同、温度分别为T1和T2的两个密闭容器中分别充入等量NO2,发生反应:2NO2(g)?N2O4(g)△H<0.恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1和a2;已知T1<T2,则a1 a2.
A.大于 B.小于 c.等于 D.以上都有可能
(5)标准状况下,将干燥纯净的氨和二氧化氮气体分别完成喷泉实验后所得溶液等体积混合,反应后溶液中的离子浓度关系正确的是 .
A.c(NO-3)>c(NH+4)>c(H+)>c(OH-)
B.c(NH+4)>c(NO-3)>c(OH-)>c(H+)
C.c(H+)=c(OH-)+c(NH3.H2O)
D.c(NH4+)+c(NH3.H2O)=1.5c(NO-3)
(1)一定条件下,向一个2L的密闭容器中充入2molN2和6molH2,反应达平衡时放出93kJ热量,生成NH3的浓度为1mol/L,试写出该反应的热化学方程式
(2)现有一支l0mL的试管,充满NO倒置于水槽中,向试管中缓缓通A-定量氧气,当试管内液面稳定时,剩余气体2mL.则通入氧气的体积可能为
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2g)?4NO(g)+6H2O(g).
| 起始浓度(mol. L-1) | c( NH3) | c( O2) | c( NO) | c( H20) |
| 甲 | 1 | 2 | 0 | 0 |
| 乙 | 2 | 4 | 0 | 0 |
| 丙 | 0.5 | x | y | z |
②恒温恒容下,若要使丙与甲平衡时各组分浓度相同,则x=
(4)向容积相同、温度分别为T1和T2的两个密闭容器中分别充入等量NO2,发生反应:2NO2(g)?N2O4(g)△H<0.恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1和a2;已知T1<T2,则a1
A.大于 B.小于 c.等于 D.以上都有可能
(5)标准状况下,将干燥纯净的氨和二氧化氮气体分别完成喷泉实验后所得溶液等体积混合,反应后溶液中的离子浓度关系正确的是
A.c(NO-3)>c(NH+4)>c(H+)>c(OH-)
B.c(NH+4)>c(NO-3)>c(OH-)>c(H+)
C.c(H+)=c(OH-)+c(NH3.H2O)
D.c(NH4+)+c(NH3.H2O)=1.5c(NO-3)
某化学兴趣小组同学在馓“证明海带中存在碘元素”的实验时,对课本上的描述:“海带灼烧后的灰烬中碘元素以I-形式存在”产生了疑问.久置KI固体被氧化变质,呈浅黄色(有I2),KI固体直接加热时,为什么不被氧化呢?因此,小组同学针对I-被氧化条件除了氧气之外还需要什么条件进行了实验探究.
提出假设:根据久置KI固体会被氧化而变质,结合空气的成分,首先排除 和稀有气体的影响.然后对KI变质条件提出合理假设:
假设一:需要H2O的参与;
假设二:需要CO2的参与;
假设三: .
实验验证:(1)为了验证假设二,小组同学设计了以下实验方案;取10mLKI溶液(浓度较大)于5支试管中,向试管中通入CO2气体或者滴加盐酸.一段时间后对比试管中的颜色深浅,之后向试管中滴入淀粉溶液,再次对比试管中的颜色深浅,具体实验现象见下表:
小组同学通过实验现象深入思考了CO2在反应过程中的作用,得出结论:CO2气体同盐酸一样在KI被氧化的过程中提供 环境.写出此实验中CO2与KI反应的化学方程式 .
(2)为了验证I-被氧化是否必须要有H2O的参与,小组同学设计了以下实验验证:
交流提高:由于空气中CO2和水蒸气的含量很低,导致在加热KI的过程中这两种气体很容易被“驱散”,不能很好地与KI接触,KI自然就不能被氧化.长时间保存碘化钾需要避光、 .
提出假设:根据久置KI固体会被氧化而变质,结合空气的成分,首先排除
假设一:需要H2O的参与;
假设二:需要CO2的参与;
假设三:
实验验证:(1)为了验证假设二,小组同学设计了以下实验方案;取10mLKI溶液(浓度较大)于5支试管中,向试管中通入CO2气体或者滴加盐酸.一段时间后对比试管中的颜色深浅,之后向试管中滴入淀粉溶液,再次对比试管中的颜色深浅,具体实验现象见下表:
| 试管序号 | 1 | 2 | 3 | 4 | 5 |
| 通入CO2时间/min | 0 | 1 | 5 | ||
| 滴加盐酸/滴 | 0 | 3 | 6 | ||
| 溶液中颜色对比 | 无色 | 浅黄色→黄色(依次加深) | |||
| 滴加淀粉溶液后的颜色对比 | 无色 | 浅蓝色→蓝色(依次加深) | |||
(2)为了验证I-被氧化是否必须要有H2O的参与,小组同学设计了以下实验验证:
| 实验步骤 | 预期现象和结论 |
| ①取一份纯净的KI固体,分成两等份; | / |
| ②一份加入到装有 一份加入到装有 ③几天后观察. |
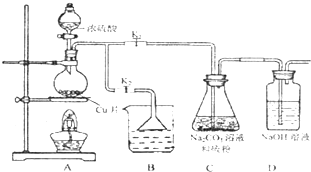 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在.
(1)某研究小组设计了制备Na2S203_5H20装置和部分操作步骤如图.
I.打开K1关闭K2,向圆底烧瓶中加入足量浓硫酸,加热.
II.C中混合液被气流搅动,反应一段时间后,硫粉的域逐渐减少,当C中溶液的pH 接近7时,打开K2,关闭K1即停止C中的反应,停止加热.
III.过滤C中的混合液.
IV.将滤液经过
①II中,“当C中溶液的pH接近7时即停止C中的反应”的原因是
②IV中,操作步骤是
③装置B中盛放的试剂是(填化学式)
④有一小组在实验中发现,二氧化硫气体产生缓慢以致后续现象不明显,但又不存在气密性问题,请你推测可能的原因
(2)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO
2- 4 |
2- 7 |
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
①Cr2O
2- 7 |
②I2+2S2O
2- 3 |
2- 6 |
则判断达到滴定终点的现象是
工业上以软锰矿为原料,利用烧结烟气中的SO2制备MnSO4?H2O的流程如下:
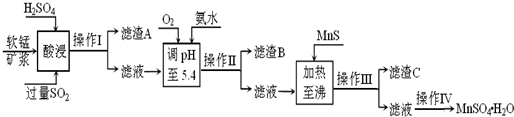
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.酸浸过程发生反应:MemOn+H+→Me(2n/m)++H2O,Me表示Fe、Al、Zn、Cu等.25℃时部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表:
回答下列问题:
(1)酸浸时SO2将MnO2还原为MnSO4,其离子方程式为 .酸浸时SO2的吸收率与pH和温度的关系如下图,为提高SO2的吸收率,酸浸适宜的条件是 .

(2)滤渣B的主要成分是 .
(3)加入MnS的目的是 .
(4)操作IV的步骤为 、 、过滤、洗涤、干燥.
(5)MnO2的生产方法之一是以石墨为电极,在不断搅拌情况下,电解酸化的MnSO4溶液,阳极的电极反应式为: .
(6)已知金属离子浓度小于1.0×10-5mol/L时认为已经完全沉淀,根据表格数据,计算25℃时Zn(OH)2溶度积Ksp为 (不需计算过程).
0 22275 22283 22289 22293 22299 22301 22305 22311 22313 22319 22325 22329 22331 22335 22341 22343 22349 22353 22355 22359 22361 22365 22367 22369 22370 22371 22373 22374 22375 22377 22379 22383 22385 22389 22391 22395 22401 22403 22409 22413 22415 22419 22425 22431 22433 22439 22443 22445 22451 22455 22461 22469 203614

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.酸浸过程发生反应:MemOn+H+→Me(2n/m)++H2O,Me表示Fe、Al、Zn、Cu等.25℃时部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(1)酸浸时SO2将MnO2还原为MnSO4,其离子方程式为

(2)滤渣B的主要成分是
(3)加入MnS的目的是
(4)操作IV的步骤为
(5)MnO2的生产方法之一是以石墨为电极,在不断搅拌情况下,电解酸化的MnSO4溶液,阳极的电极反应式为:
(6)已知金属离子浓度小于1.0×10-5mol/L时认为已经完全沉淀,根据表格数据,计算25℃时Zn(OH)2溶度积Ksp为