反应4NH3+5O2?4NO+6H2O在5L密闭容器中进行,10秒钟后NO的物质的量增加了5mol,则此反应的平均速率v为( )
| A、v(O2)=0.1mol?L-1?s-1 | B、v(NO)=0.1mol?L-1?s-1 | C、v(H2O)=0.03mol?L-1?s-1 | D、v(NH3)=0.01mol?L-1?s-1 |
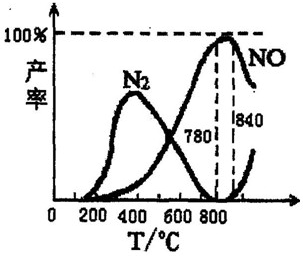 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图.
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图.①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ/mol
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ/mol
下列说法中不正确的是( )
| A、N2(g)+O2(g)?2NO(g);△H=+181.5 kJ/mol | B、加压有利于NH3生成NO,不利于NH3生成N2 | C、工业上氨催化氧化生成NO时,温度应控制在780~840℃之间 | D、工业上通常提高氧气的浓度,以提高NH3的转化率 |
一定条件下,一固定容积的密闭容器中发生反应:2A2(g)+B2(s)?2C3(g);△H=-a kJ/mol(a>0),能说明该反应已经达到平衡状态的是( )
| A、2v逆(A2)=v正(B2) | B、反应中消耗2molA2同时生成2molC3 | C、容器内混合气体的密度保持不变 | D、容器内压强保持不变 |
在一定温度下的定容密闭容器中,对于反应A(s)+2B(g)?C(g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是( )
| A、混合气体的压强 | B、混合气体的密度 | C、混合气体的总体积 | D、气体总物质的量 |
一定温度下,某密闭容器中充入等物质的量的气体A和B,发生如下反应:A(g)+xB(g)?2C(g)
达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如图所示.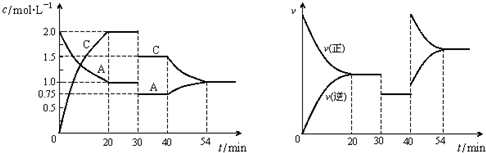
下列说法中正确是( )
达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如图所示.

下列说法中正确是( )
| A、0~20 min内用A的浓度变化表示的平均反应速率为0.05 mol/(L?min) | B、30~40 min改变的条件是将容器的体积扩大至原来的2倍 | C、一定条件下,当v(B)正:v(C)逆=1:2时的状态即为化学平衡状态 | D、若25 min、35 min、55 min时的化学平衡常数分别为K1、K2、K3,则K3>K2=K1 |
盐酸与碳酸钙反应时,下列措施能使最初的反应速率明显加快的是( )
| A、增加碳酸钙的量 | B、盐酸的用量增加一倍 | C、盐酸用量减半 | D、温度升高30℃ |