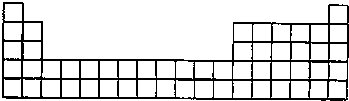
四种短周期元素在周斯表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.下列说法正确的是( )
| X | Y | |
| Z | W |
| A、元素Z位于周期表中第二周期,ⅤA族 |
| B、W元素最高价氧化物的水化物酸性是同周期最强的 |
| C、这些元素中,Y的氢化物水溶液碱性最强 |
| D、四种元素中原子半径最大的为W |
短周期元素W、X、Y和Z的原子序数依次增大,W原子形成的单质是密度最小的气体,X原子的最外层电子数是内层电子数的2倍,Y原子的最外层电子数是其电子层数的3倍,元素Z是地壳中含量最多的金属元素.下列说法不正确的是( )
| A、元素X与W形成的原子个数比为1:1的化合物有多种 | B、Y与Z的简单离子的半径大小是Yn-<Zm+ | C、元素Z的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | D、元素Y可与元素X形成直线型化合物XY2 |
短周期主族元素A、B、C、D的原子序数依次增大.A、C原子序数相差8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A、原子半径:A<D<C<B | B、B、C、D分别与A形成的化合物一定含有相同的化学键 | C、最高价氧化物对应水化物的酸性:D<C | D、常温下,单质B能大量溶于浓硝酸中 |
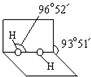 (1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是(2)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
(4)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:R3+
| OH- |
| H+ |
| ||
| H+ |
①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键.
研究物质的微观结构,有助于人们理解物质性质和变化的本质.请回答下列问题.
(1)CH4中H为+1价,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序是: .
(2)A、B均为短周期金属元素.依据下表数据和已学知识,写出B原子的电子排布式: .
(3)CO与Cl2在催化剂作用下生成COCl2,COCl2俗称光气,极毒,光气分子呈平面三角形,结构式为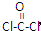 ,COCl2分子内含有 (填标号)
,COCl2分子内含有 (填标号)
A.4个σ键 B.2个σ键、2个π键
C.3个σ键、1个π键 D.2个σ键、1个π键.
0 22152 22160 22166 22170 22176 22178 22182 22188 22190 22196 22202 22206 22208 22212 22218 22220 22226 22230 22232 22236 22238 22242 22244 22246 22247 22248 22250 22251 22252 22254 22256 22260 22262 22266 22268 22272 22278 22280 22286 22290 22292 22296 22302 22308 22310 22316 22320 22322 22328 22332 22338 22346 203614
(1)CH4中H为+1价,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序是:
(2)A、B均为短周期金属元素.依据下表数据和已学知识,写出B原子的电子排布式:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
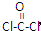 ,COCl2分子内含有
,COCl2分子内含有A.4个σ键 B.2个σ键、2个π键
C.3个σ键、1个π键 D.2个σ键、1个π键.