在一密闭容器中进行反应:X2+3Y2?2Z2,若X2、Y2、Z2的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,当反应达到平衡状态时,下列物质的浓度可能为( )
| A、X2为0.2 mol/L | B、Y2为0.2 mol/L | C、Z2为0.4 mol/L | D、Y2为0.6 mol/L |
在固定体积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程某一时刻SO2,O2,SO3浓度(mol/L)分别为0.2,0.2,0.2,达到平衡时,浓度可能正确的是( )
| A、SO2,O2分别为0.4,0.3mol/L | B、SO2为0.25mol/L | C、SO2,SO3均为0.15mol/L | D、SO3为0.4mol/L |
某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图I所示,若其它条件不变,当 温度分别为T1和T2时,Y的体积分数与时间关系如图II所示.则下列结论正确的是( )
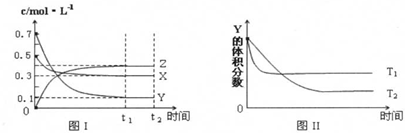

| A、该反应的热化学方程式为:X(g)+3Y(g)?2Z(g);△H>0 | B、若其它条件不变,升高温度,正、逆反应速率均增大,X的转化率减小 | C、达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动 | D、达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
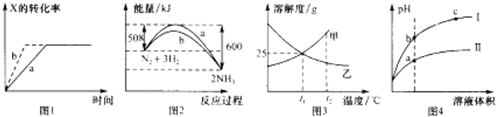
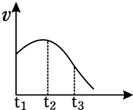 将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( )
将除去氧化膜的镁条投入到少量稀盐酸中进行实验,实验测得氢气的产生速率变化情况如图曲线所示,对该曲线的解释中正确的是( )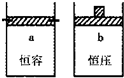 一定温度下,往a、b两容器中各注入1mol三氧化硫,a、b两容器起始体积和压强均相同,分别保持恒容和恒压,发生以下反应:2SO3(g)
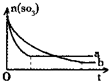
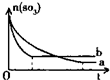
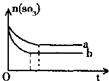
一定温度下,往a、b两容器中各注入1mol三氧化硫,a、b两容器起始体积和压强均相同,分别保持恒容和恒压,发生以下反应:2SO3(g)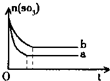
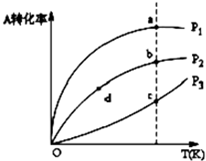 密闭容器中,发生反应A(g)+2B(g)?C(g)+D(g),反应开始时加入的各反应物的量相同,测得A在不同压强、不同温度下的平衡转化率与温度的关系如图所示.下列说法正确的是( )
密闭容器中,发生反应A(g)+2B(g)?C(g)+D(g),反应开始时加入的各反应物的量相同,测得A在不同压强、不同温度下的平衡转化率与温度的关系如图所示.下列说法正确的是( )