题目内容
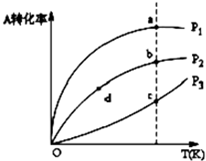 密闭容器中,发生反应A(g)+2B(g)?C(g)+D(g),反应开始时加入的各反应物的量相同,测得A在不同压强、不同温度下的平衡转化率与温度的关系如图所示.下列说法正确的是( )
密闭容器中,发生反应A(g)+2B(g)?C(g)+D(g),反应开始时加入的各反应物的量相同,测得A在不同压强、不同温度下的平衡转化率与温度的关系如图所示.下列说法正确的是( )分析:A.该反应正反应是体积减小的反应,压强越大,A的转化率越大;
B.b、d处于等压线上,温度越高反应速率越快;
C.由图可知,压强一定,温度越高A的转化率越高,说明升高温度平衡向正反应移动;
D.压强越大平衡时反应混合物的总的物质的量越小,混合气体的总质量不变,据此判断.
B.b、d处于等压线上,温度越高反应速率越快;
C.由图可知,压强一定,温度越高A的转化率越高,说明升高温度平衡向正反应移动;
D.压强越大平衡时反应混合物的总的物质的量越小,混合气体的总质量不变,据此判断.
解答:解:A.该反应正反应是体积减小的反应,压强越大,A的转化率越大,由图可知,转化率α(P1)>α(P2)>α(P3),故压强:P1>P2>P3,故A错误;
B.b、d处于等压线上,曲线上各点都是平衡点,b点温度高,升高温度正、逆增大,故平衡时正、逆反应速率v(b)都一定大于v(d),故B正确;
C.由图可知,压强一定,温度越高A的转化率越高,说明升高温度平衡向正反应移动,平衡常数增大,故平衡常数:K(c)>K(d),故C正确;
D.混合气体的总质量不变,压强:P1>P3,压强越大平衡时反应混合物的总的物质的量越小,故气体平均摩尔质量:M(a)>M(c),故D正确;
故选BCD.
B.b、d处于等压线上,曲线上各点都是平衡点,b点温度高,升高温度正、逆增大,故平衡时正、逆反应速率v(b)都一定大于v(d),故B正确;
C.由图可知,压强一定,温度越高A的转化率越高,说明升高温度平衡向正反应移动,平衡常数增大,故平衡常数:K(c)>K(d),故C正确;
D.混合气体的总质量不变,压强:P1>P3,压强越大平衡时反应混合物的总的物质的量越小,故气体平均摩尔质量:M(a)>M(c),故D正确;
故选BCD.
点评:本题考查化学平衡图象、影响化学平衡的因素等,难度中等,注意利用“定一议二”原则分析解答.

练习册系列答案
相关题目
 2HI(g).
2HI(g).