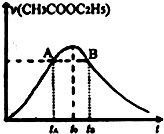
 乙酸乙酯能在多种条件下发生水解反应:
乙酸乙酯能在多种条件下发生水解反应:CH3COOC2H5+H2O?CH3COOH+C2H5OH
已知该反应的速率随c(H+)的增大而加快.如图为CH3COOC2H5的水解速率随时间的变化图.下列说法中正确的是( )
| A、反应初期水解速率增大可能是溶液中c(H+)逐渐增大所致 | B、A、B两点表示的c(CH3COOC2H5)相等 | C、图中t0时反应达到平衡状态 | D、tB时CH3COOC2H5的转化率高于tA时CH3COOC2H5的转化率 |
一定条件下,在一定体积的密闭容器中一定量的物质A、B发生反应:aA(g)+bB(g)?xC(g)达到化学平衡,并有图1所示的变化关系,其中C%表示平衡混合气中C的体积分数,T为温度,ρ为压强,t为时间.则在图2中,Y轴表示的是( )
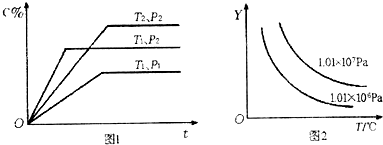

| A、平衡混合气中A或C的体积分数 | B、平衡混合气的密度 | C、平衡时,A或B的转化率 | D、平衡时,C的物质的量浓度 |
下列事实不能用勒夏特列原理解释的是( )
| A、打开汽水瓶有气泡从溶液中冒出 | B、实验室用排饱和食盐水法收集氯气 | C、合成氨工厂学采用增大压强以提高原料的利用率 | D、由H2、I2(g)、HI气体组成的平衡减压后颜色变浅 |
下列事实不能用勒夏特列原理解释的是( )
| A、氯化铁溶液加热蒸干最终得不到氯化铁固体 | B、工业上合成氨采用较高的温度 | C、常温下,将1mol pH=3的醋酸溶液加水稀释至100ml,测得其PH<5 | D、钠与氯化钾共融制备钾:Na(l)+KCl(l)?K(g)+NaCl(l) |
合成氨时采用500℃左右的温度进行,主要是因为该温度时( )
| A、合成氨的反应速率最大 | B、H2的转化率最高 | C、催化剂的活性最大 | D、N2的转化率最高 |
Fe2O3+3CO
2Fe+3CO2 是炼铁高炉中发生的一个可逆反应.早在19世纪的欧洲,炼铁工程师就发现在其他条件不变时,增加高炉的高度,高炉尾气中CO的比例竟然没有改变.关于这一事实,下列说法不合理的是( )
| 高温 |
| A、一定条件下,任何可逆反应的进程都有一定的限度,所以CO不可能完全转化 |
| B、尾气中CO的比例不变,说明反应达到了这一条件下的化学平衡状态 |
| C、尾气中CO的比例不变,是因为CO 的消耗速率与CO 生成速率相等 |
| D、CO是气体,铁矿石(主要成分Fe2O3)是固体,CO 与铁矿石接触不充分 |
高炉炼铁时,当发现炼铁炉口排出的尾气中CO的含量过高,为提高反应中CO的利用率,采取下列哪个措施一定是徒劳的( )
| A、提高炉温 | B、增高炉的高度 | C、加大原料铁矿石的投放量 | D、增加气体压强 |
在温度,容积相同的3个密闭容器中,按不同方式投入反应物,在保持恒温、恒容条件下发生如下反应:3X(g)+Y(g)?2Z(g)△H<0,测得相关数据如下表:
|