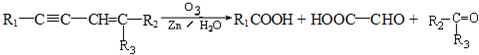题目内容
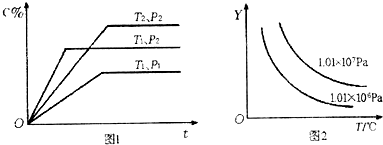
一定条件下,在一定体积的密闭容器中一定量的物质A、B发生反应:aA(g)+bB(g)?xC(g)达到化学平衡,并有图1所示的变化关系,其中C%表示平衡混合气中C的体积分数,T为温度,ρ为压强,t为时间.则在图2中,Y轴表示的是( )

| A、平衡混合气中A或C的体积分数 | B、平衡混合气的密度 | C、平衡时,A或B的转化率 | D、平衡时,C的物质的量浓度 |
分析:根据图1中“先拐先平数值大”知,T1>T2,P2>P1,升高温度,C的含量降低,说明该反应向逆反应方向移动,则正反应是放热反应,增大压强,C的含量增大,平衡向正反应方向移动,则该反应是一个反应前后气体体积减小的反应.
解答:解:根据图1中“先拐先平数值大”知,T1>T2,P2>P1,升高温度,C的含量降低,说明该反应向逆反应方向移动,则正反应是放热反应,增大压强,C的含量增大,平衡向正反应方向移动,则该反应是一个反应前后气体体积减小的反应;
A.根据图2知,增大压强,平衡向正反应方向移动,则A的体积分数减小,与图象不相符,故A错误;
B.在一定温度下,根据质量守恒知,混合气体的质量始终不变,容器体积不变,则混合气体的密度始终不变,故B错误;
C.升高温度平衡向逆反应方向移动,则A或B的转化率减小,增大压强平衡正反应方向移动,A或B的转化率增大,所以符合图象,故C正确;
D.升高温度平衡向逆反应方向移动,C的物质的量浓度减小,增大压强平衡正反应方向移动,C的物质的量浓度增大,所以符合图象,故D正确;
故选CD.
A.根据图2知,增大压强,平衡向正反应方向移动,则A的体积分数减小,与图象不相符,故A错误;
B.在一定温度下,根据质量守恒知,混合气体的质量始终不变,容器体积不变,则混合气体的密度始终不变,故B错误;
C.升高温度平衡向逆反应方向移动,则A或B的转化率减小,增大压强平衡正反应方向移动,A或B的转化率增大,所以符合图象,故C正确;
D.升高温度平衡向逆反应方向移动,C的物质的量浓度减小,增大压强平衡正反应方向移动,C的物质的量浓度增大,所以符合图象,故D正确;
故选CD.
点评:本题考查了温度、压强对化学平衡的影响,根据图1确定该反应的反应热、气体体积系数之间的关系,再结合图2中温度、压强对化学平衡的影响来分析解答,难度中等.

练习册系列答案
相关题目
 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)

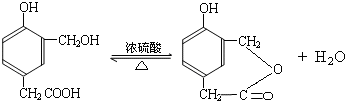
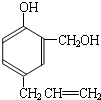
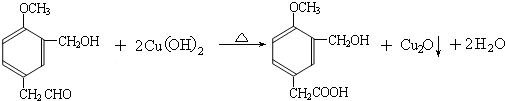
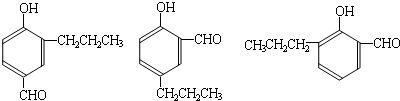
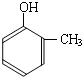 到的合成
到的合成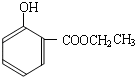 路线(用合成路线流程图表示,并注明反应条件).
路线(用合成路线流程图表示,并注明反应条件).