反应4NH3+5O2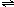 4NO+6H2O在5升的密闭容器中进行,半分钟后,NO的物质的量增加了0.3摩尔,则此反应的平均速度
4NO+6H2O在5升的密闭容器中进行,半分钟后,NO的物质的量增加了0.3摩尔,则此反应的平均速度
(表示反应物的消耗速度或生成物的生成速度)为( )
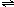 4NO+6H2O在5升的密闭容器中进行,半分钟后,NO的物质的量增加了0.3摩尔,则此反应的平均速度
4NO+6H2O在5升的密闭容器中进行,半分钟后,NO的物质的量增加了0.3摩尔,则此反应的平均速度. |
| Vx |
A、
| ||
B、
| ||
C、
| ||
D、
|
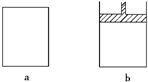 有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变.在同温同压和等体积条件下,向a和b两容器中通入等物质的量的
有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变.在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应:2NO2?N2O4(正反应放热),则以下说法正确的是( )?
| A、反应起始时反应速率的关系:va<vb? | B、反应过程中反应速率的关系:va<vb? | C、两容器内反应达到平衡所需时间一定相同? | D、反应达到平衡,两容器中的NO2的转化率相同? |
某化学反应2X(g)?Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol.L-1)随反应时间(min)的变化情况如下表:
下列说法不正确的是( )
| 实验 序号 |
时间 浓度 温度 |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A、前10分钟,实验4的平均化学反应速率比实验1的大 |
| B、实验2可能使用了催化剂 |
| C、C>1.0 |
| D、实验3比实验2先达到化学平衡状态 |
化学反应H2(g)+I2(g)?2HI(g)在持续加热的条件下,向密闭容器中充入2mol H2和3mol I2(g),充分反应后,该密闭容器中( )
| A、2 mol H2已耗尽 | B、3 mol I2(g)已耗尽 | C、HI的物质的量等于4 mol | D、HI的物质的量少于4 mol |
在固定体积的密闭容器中进行如下反应:2AB2(g)+B2(g)?2AB3(g).已知反应过程某一时刻AB2、B2、AB3浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,达到平衡时,浓度可能正确的是( )
| A、AB2、B2分别为0.4mol/L、0.2mol/L | B、AB2为0.25mol/L | C、AB2、AB3均为0.15mol/L | D、AB3为0.4mol/L |
可逆反应2SO2+O2?2SO3,若用2mol SO2和1mol 18O2在一定条件下,经足够长的时间反应,下列情况可能出现的是( )
| A、容器中只有三氧化硫 | B、18O原子存在于氧气、二氧化硫、三氧化硫中 | C、生成2 mol 三氧化硫 | D、18O原子只存在于三氧化硫与氧气中 |
在密闭容器中进行X2(气)+3Y2(气)?2Z(气)的反应,X2、Y2、Z的起始浓度依次为0.1mol/L、0.3mol/L、0.2mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
| A、C(Z):0.5mol/L | B、C(Y2)=0.5mol/L | C、C(Z)=0 | D、C(X2)=0.2mol/L |
下列不可能属于可逆反应的是( )
| A、氯气与水反应生成盐酸与次氯酸 | B、N2与H2在一定条件下可以生成NH3,同时NH3又可分解为N2和H2 | C、电解水生成H2和O2,氢气和氧气转化成H2O | D、SO2溶于水和H2SO3分解 |
所有化学平衡都是一种动态平衡,下列说法中不正确的是( )
| A、在合成氨的平衡体系中,一定存在N2、H2、NH3三种物质 | B、BaSO4的沉淀溶解平衡中,不存在溶解的BaSO4分子 | C、在醋酸溶液中,一定存在H+、OH-、CH3COO-、CH3COOH分子、H2O分子 | D、往平衡体系FeCl3+3KSCN?Fe(SCN)3+3KCl中加入KCl固体,平衡将向逆反应方向移动,溶液颜色将变浅 |
在给定条件下,下列加点的物质在化学反应中能完全消耗的是( )
A、在5×107Pa、500℃和铁触媒催化的条件下,用1mol
| ||||
B、标准状况下,将1g
| ||||
C、向150mL 3mol?L-1的硝酸中加入6.4g
| ||||
D、用50mL 8mol?L-1浓
|