题目内容
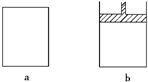 有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变.在同温同压和等体积条件下,向a和b两容器中通入等物质的量的
有两个极易导热的密闭容器a和b(如图所示),a容器体积恒定,b容器体积可变,压强不变.在同温同压和等体积条件下,向a和b两容器中通入等物质的量的NO2,发生反应:2NO2?N2O4(正反应放热),则以下说法正确的是( )?
| A、反应起始时反应速率的关系:va<vb? | B、反应过程中反应速率的关系:va<vb? | C、两容器内反应达到平衡所需时间一定相同? | D、反应达到平衡,两容器中的NO2的转化率相同? |
分析:A、根据浓度、温度、压强对反应速率的影响分析;
B、温度不变,根据方程式中气体物质的量变化结合容器体积特点分析两容器内压强关系,压强越大,反应速率越快;
C、速率越快,到达平衡的时间越短;
D、温度不变,根据方程式中气体物质的量变化结合容器体积特点分析两容器内压强关系.
B、温度不变,根据方程式中气体物质的量变化结合容器体积特点分析两容器内压强关系,压强越大,反应速率越快;
C、速率越快,到达平衡的时间越短;
D、温度不变,根据方程式中气体物质的量变化结合容器体积特点分析两容器内压强关系.
解答:解:A、反应起始时,二氧化氮的浓度相同、温度相同、压强相同,反应速率Va=Vb,故A错误;
B、容器a体积不变,随反应进行,反应混合气体的物质的量减小,容器a中压强降低,容器b体积可变,压强不变,压强越大,反应速率越快,故v(a)<v(b),故B正确;
C、速率越快,到达平衡的时间越短,故容器b到达平衡所用时间少,故C错误;
D、容器a体积不变,随反应进行,反应混合气体的物质的量减小,容器a中压强降低,容器b体积可变,压强不变,故反应达到平衡时,两容器内的压强关系是p(a)<p(b),b中二氧化氮转化率增大,两容器中的NO2的转化率不相同,故D错误;
故选B.
B、容器a体积不变,随反应进行,反应混合气体的物质的量减小,容器a中压强降低,容器b体积可变,压强不变,压强越大,反应速率越快,故v(a)<v(b),故B正确;
C、速率越快,到达平衡的时间越短,故容器b到达平衡所用时间少,故C错误;
D、容器a体积不变,随反应进行,反应混合气体的物质的量减小,容器a中压强降低,容器b体积可变,压强不变,故反应达到平衡时,两容器内的压强关系是p(a)<p(b),b中二氧化氮转化率增大,两容器中的NO2的转化率不相同,故D错误;
故选B.
点评:本题考查了化学反应速率的影响因素等,难度不大,注意题目实际为恒温条件,分析两容器中压强的变化是关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
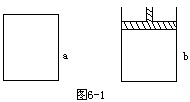
 N2O4
△H<0,则以下说法正确的是
N2O4
△H<0,则以下说法正确的是
 N2O4
△H<0,则以下说法正确的是:(
)
N2O4
△H<0,则以下说法正确的是:(
)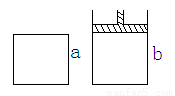
 N2O4+Q(Q>0),请用“> ”、“<”或“=”填空:
N2O4+Q(Q>0),请用“> ”、“<”或“=”填空: