某种氢氧燃料电池应用于潜艇中的电极反应式为:负极:2H2-4e-+4OH-?4H2O;正极:O2+4e-+2H2O?4OH-,所产生的水还可作为饮用水.今欲得到常温下1L水,则电池内转移电子的物质的量约为( )
| A、8.9×10-3mol | B、4.5×10-2mol | C、1.1×102mol | D、5.6×10-3 mol |
钢铁在下列哪种情况下最容易生锈( )
| A、在干燥的氧环境中 | B、在潮湿无氧环境中 | C、制成不锈钢 | D、蘸有食盐水暴露在空气中 |
下列事实与电化学腐蚀无关的是( )
| A、钢铁制品生锈后用盐酸处理 | B、黄铜(Cu、Zn合金)制的铜锣不易产生铜绿 | C、铜、铝电线一般不连接起来作导线 | D、生铁比熟铁(几乎是纯铁)容易生绣 |
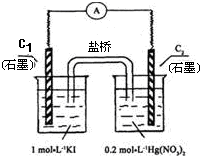 硝酸汞和碘化钾溶液混合后会生成红色的碘化汞沉淀,为了探究硝酸汞和碘化钾溶液之间能否发生氧化还原反应,研究人员设计了如图的实验装置,结果电流计指针发生了偏转,下列分析正确的是( )
硝酸汞和碘化钾溶液混合后会生成红色的碘化汞沉淀,为了探究硝酸汞和碘化钾溶液之间能否发生氧化还原反应,研究人员设计了如图的实验装置,结果电流计指针发生了偏转,下列分析正确的是( )| A、如图装置的电流方向是从C1到C2 | B、C1是负极,发生的反应是2I-?I2+2e- | C、K+离子向C1电极流动 | D、装置发生的总反应是Hg2++2I-?HgI2↓ |
锌-空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性.在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2+2H2O.下列有关锌-空气电池说法正确的是( )
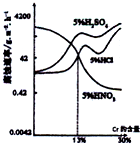 右图是三种酸对Fe-Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是( )
右图是三种酸对Fe-Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是( )| A、稀硫酸对Fe-Cr合金的腐蚀性比稀硝酸和稀盐酸都强 | B、随着Fe含量的增加,Fe-Cr合金在5%HNO3中的耐腐蚀性越来越弱 | C、Cr含量等于13%时,三种酸对Fe-Cr合金的腐蚀速率由快到慢的顺序为H2SO4>HCl=HNO3 | D、Cr含量小于13%时,因为三种酸中硫酸的氢离子浓度最大,所以对Fe-Cr合金的腐蚀性最强 |
有一可充-放电的锂离子电池,放电时负极反应为:LiC6-e-?6C+Li+,正极反应:CoO2+Li++e-?LiCoO2,下列说法正确的是( )
| A、放电时Li+向负极移动 | B、该电池可以采用水溶液做电解质,也可以用有机溶剂 | C、充电时LiCoO2作阳极 | D、充电时若有1mol电子转移,则阴极消耗1mol LiC6 |
下列关于化学与生产、生活的认识正确的是( )
| A、镀锌铁键层破损后,铁更容易被腐烛 | B、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 | C、用磷酸钙陶瓷制造人体骨骼,这是利用该材料的生物功能 | D、汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 |
甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电流正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙.则下列叙述正确的是( )
| A、甲、丙中是化学能转变为电能,乙中是电能转变为化学能 | B、C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 | C、C1和C3放出的气体相同,铜片和铁片放出的气体也相同 | D、甲、乙中溶液的pH值逐渐升高,丙中溶液的pH逐渐减小 |
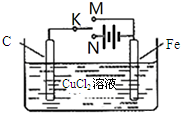 某学习小组为研究电化学原理,设计右图装置.下列叙述正确的是( )
某学习小组为研究电化学原理,设计右图装置.下列叙述正确的是( )