某化学兴趣小组同学受“铝-空气-海水电池”的启发,在老师的指导下用易拉罐(铝合金)、家庭常用的漂白水、食盐、氢氧化钠、石墨电极(从废旧干电池中获得)等原料制作了一个原电池.电池的总反应方程式为2A1+3C10-?+20H-??3C1-?+2Al
+H20.下列说法不正确的是( )
| O | - 2 |
A、该电池的负极反应式为2Al+80H-?-6e-??2Al
| ||
| B、该电极的正极反应式为3C10-?+3H20+6e-?3Cl-?+60H-? | ||
| C、外电路中电子从石墨电极流向易拉罐 | ||
| D、当有0.1 mol Al完全溶解时,流经外电路的电子个数约为1.806×1023 |
微生物燃料电池因具有原料广泛、操作条件温和、资源利用率高、对环境无污染等特点而被人们重视,以用葡萄糖作底物的燃料电池为例,其正、负极反应式如下:
正极6O2+24H++24e-
12H20
负极C6H12O6+6H2O-24e-
6CO2↑+24H+
则下列有关该电池的说法正确的是( )
正极6O2+24H++24e-
| ||
负极C6H12O6+6H2O-24e-
| ||
则下列有关该电池的说法正确的是( )
| A、该电池的工作环境是高温条件 | ||||
| B、葡萄糖(C6H12O6)在变化中失去电子,被还原 | ||||
| C、该电池的电解质溶液是强酸性溶液,如浓硫酸等 | ||||
D、该电池的总反应式为C6H1206+602
|
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为C0,但实际上乙醇被氧化为乙醛或乙酸,下列关于乙醇被氧化成乙醛和乙酸两种情况的说法正确的是( )
| A、乙醇都是在正极上发生氧化反应,电流经外电路流向负极 | B、检测室里电解质溶液中的H+都是向负极移动 | C、当乙醇被氧化成乙醛时,正极反应式为02+4e-+2H20?40H-? | D、当乙醇被氧化成乙酸时,负极反应式为CH3CH0H-4e-+H20?CH3COOH+4H+ |
25℃、101kPa下:
①2Na(s)+
O2(g)═Na2O(s)△H1=-414kJ/mol;
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol.
下列说法正确的是( )
①2Na(s)+
| 1 |
| 2 |
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol.
下列说法正确的是( )
| A、①和②生成等物质的量的产物,转移的电子数相同 |
| B、Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| C、25℃、101 kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=+317 kJ/mol |
| D、①和②产物中的阴阳离子个数比均为1:1 |
LiH可作飞船的燃料,已知下列反应:
①2Li(S)+H2(g)═2LiH(s)△H=-182kJ?mol-1;
②2H2(g)+O2(g)═2H2O(1)△H=-572kJ?mol-1;
③4Li(s)+O2(g)═2Li2O(s)△H=-1196kJ?mol-1.
则LiH在O2中燃烧的热化学方程式为( )
①2Li(S)+H2(g)═2LiH(s)△H=-182kJ?mol-1;
②2H2(g)+O2(g)═2H2O(1)△H=-572kJ?mol-1;
③4Li(s)+O2(g)═2Li2O(s)△H=-1196kJ?mol-1.
则LiH在O2中燃烧的热化学方程式为( )
| A、2LiH(s)+O2(g)═LiO(S)+HO(l)△H=-702 kJ?mol?? | B、2LiH(s)+O2(g)═LiO (s)+HO(l)△H=-1 950 kJ?mol?? | C、2LiH(s)+O2(g)═LiO(s)+HO(l)△H=-1 586 kJ?mol?? | D、2LiH(s)+O2(g)═LiO(s)+HO(g)△H=-988 kJ?mol?? |
2CO(g)+4H2(g)═2CH4(g)+O2(g)△H=+71kJ?mol-1??
CO(g)+2H2(g)═CH3OH(l)△H=-90.5kJ?mol-1??
已知CH4(g)的燃烧热为-890 kJ?mol-1,则CH3OH(l)的燃烧热为( )
CO(g)+2H2(g)═CH3OH(l)△H=-90.5kJ?mol-1??
已知CH4(g)的燃烧热为-890 kJ?mol-1,则CH3OH(l)的燃烧热为( )
| A、-1 528 kJ?mol-1?? | B、-764 kJ?mol-1? | C、-382 kJ?mol-1?? | D、无法计算 |
标准生成热指的是在某温度下,由处于标准状态的各种元素的最稳定的单质生成标准状态下1mol某纯物质的热效应,单位常用kJ?mol表示.已知在25℃的条件下:
Ag2O(s)+2HCl(g)═2AgCl(s)+H2O(l)△H?=-324.4kJ?mol
2Ag(s)+
O2(g)═Ag2O(s)△H?=-30.56kJ?mol
H2(g)+
Cl2(g)═HCl(g)△H?=-92.21kJ?mol??
H2(g)+
O2(g)═H2O(l)△H?=-285.6kJ?mol??
则25℃时氯化银的标准生成热为( )
Ag2O(s)+2HCl(g)═2AgCl(s)+H2O(l)△H?=-324.4kJ?mol
2Ag(s)+
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
则25℃时氯化银的标准生成热为( )
| A、-126.89 kJ?mol?? |
| B、-324.4 kJ?mol?? |
| C、-30.56 kJ?mol?? |
| D、题中数据不足,无法计算 |
已知:①1g氢气在氧气中完全燃烧生成气态水,放出热量l20.g kJ,②中和热为57.3kJ/mol,③C(石墨)═C(金刚石)△H=+1.90kJ/mol,下列说法正确的是( )
| A、氢气的燃烧热为241.8 kJ/mol | B、氢气燃烧的热化学方程式:2H2+O2一2H2O△H=-483.6 kJ/mol | C、盐酸和氨水混合的热化学方程式:H?(aq)+OH?(aq)═H2O(l)△H=-57.3 kJ/mol | D、由③可知金刚石不及石墨稳定 |
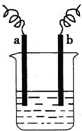 如图所示,两电极上发生的电极反应为a极2H+?+2e?═H2↑,b极.Zn═2e═Zn2+.则以下说法不正确的是( )
如图所示,两电极上发生的电极反应为a极2H+?+2e?═H2↑,b极.Zn═2e═Zn2+.则以下说法不正确的是( )