0 21242 21250 21256 21260 21266 21268 21272 21278 21280 21286 21292 21296 21298 21302 21308 21310 21316 21320 21322 21326 21328 21332 21334 21336 21337 21338 21340 21341 21342 21344 21346 21350 21352 21356 21358 21362 21368 21370 21376 21380 21382 21386 21392 21398 21400 21406 21410 21412 21418 21422 21428 21436 203614






 2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol
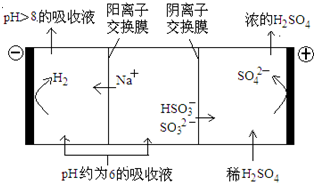 (2012?北京)直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(2012?北京)直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.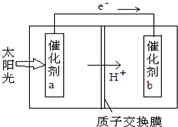 (2012?北京)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
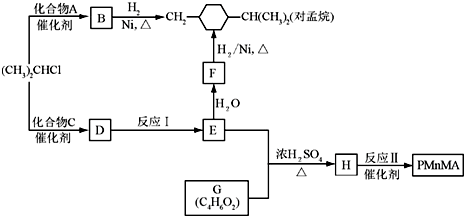
(2012?北京)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )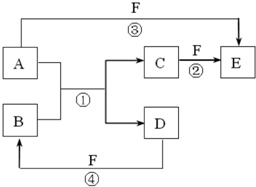 (2011?湖北模拟)A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应.
(2011?湖北模拟)A、B、C、D、E、F是中学中常见的物质,其转化关系如图所示(反应条件未标出),已知反应①是置换反应.