0 21128 21136 21142 21146 21152 21154 21158 21164 21166 21172 21178 21182 21184 21188 21194 21196 21202 21206 21208 21212 21214 21218 21220 21222 21223 21224 21226 21227 21228 21230 21232 21236 21238 21242 21244 21248 21254 21256 21262 21266 21268 21272 21278 21284 21286 21292 21296 21298 21304 21308 21314 21322 203614
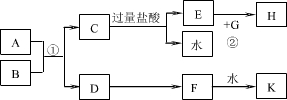
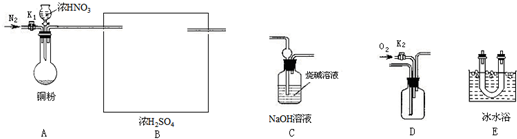

 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
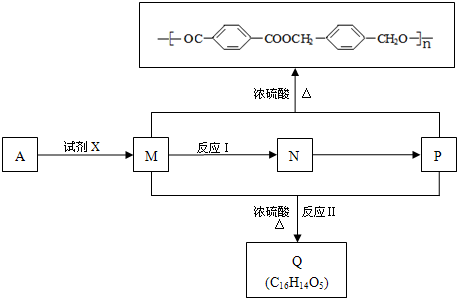

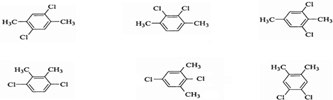 (任选一种)
(任选一种) (2011?丰台区二模)一定条件下密闭容器中的可逆反应2A(g)+B(g
(2011?丰台区二模)一定条件下密闭容器中的可逆反应2A(g)+B(g 2C(g),△H<0达到平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是
2C(g),△H<0达到平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是