题目内容
(2011?丰台区二模)某芳香化合物A的化学式为RX2(R代表烃基,X代表卤素原子),其相对分子质量为175,其分子中碳、氢元素的质量比为12:1,含X元素的质量分数为40.6%.请回答:
(1)卤代烃RX2的分子式
(2)已知:
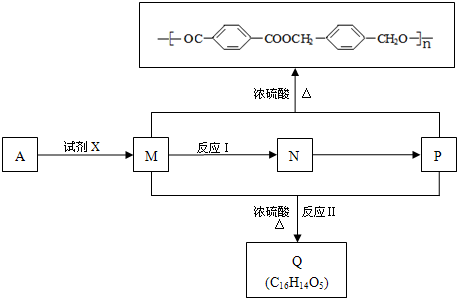
①反应Ⅰ的反应类型
②试剂X为
③反应Ⅱ的化学方程式
 .
.
(3)检验A分子中的卤素原子,简述实验方案
(4)苯环上的一溴代物只有一种,与A互为同分异构体的物质有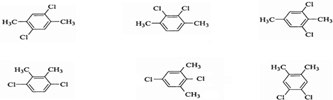 (任选一种)
(任选一种) (任选一种).
(任选一种).
(1)卤代烃RX2的分子式
C8H8Cl2
C8H8Cl2
.(2)已知:

①反应Ⅰ的反应类型
氧化反应
氧化反应
,N分子中含氧官能团的名称醛基
醛基
.②试剂X为
NaOH溶液
NaOH溶液
.③反应Ⅱ的化学方程式


(3)检验A分子中的卤素原子,简述实验方案
取少量卤代烃置于试管中,加入1mL5%的NaOH溶液,充分振荡、静置,待溶液分层后取上层水溶液,加入另一只盛有10mL稀硝酸溶液的试管中,然后加入2-3滴2%的硝酸银溶液,有白色沉淀生成.
取少量卤代烃置于试管中,加入1mL5%的NaOH溶液,充分振荡、静置,待溶液分层后取上层水溶液,加入另一只盛有10mL稀硝酸溶液的试管中,然后加入2-3滴2%的硝酸银溶液,有白色沉淀生成.
.(4)苯环上的一溴代物只有一种,与A互为同分异构体的物质有
6
6
种,写出其中一种的结构简式 (任选一种)
(任选一种) (任选一种)
(任选一种)分析:(1)根据X元素的质量分数为40.6%,则碳、氢元素的质量分数之和为59.4%,然后根据分子中碳、氢元素的质量比为12:1,求出各自的质量分数,利用碳、氢元素的质量分数以及相对分子质量为175,求出一个分子含有的C、H原子个数,最后根据相对分子质量为175,求出卤素的种类;
(2)①根据M、P发生缩聚反应可知,M为E二元醇,N为二元酸,所以M→N→P是醇连续两次氧化生成酸,N为二元醛;
②根据卤代烃在碱性条件下发生水解反应;
③根据A的分子式为C8H8Cl2,结合M、P发生缩聚反应的产物,确定各物质的结构简式,再根据醇与酸发生酯化反应来写方程式;
(3)根据卤代烃在碱性条件下发生水解反应生成氯化氢,氯化氢能与硝酸银溶液反应生成白色沉淀;
(4)根据苯环上氢原子的种类决定了一溴代物的种类来解答.
(2)①根据M、P发生缩聚反应可知,M为E二元醇,N为二元酸,所以M→N→P是醇连续两次氧化生成酸,N为二元醛;
②根据卤代烃在碱性条件下发生水解反应;
③根据A的分子式为C8H8Cl2,结合M、P发生缩聚反应的产物,确定各物质的结构简式,再根据醇与酸发生酯化反应来写方程式;
(3)根据卤代烃在碱性条件下发生水解反应生成氯化氢,氯化氢能与硝酸银溶液反应生成白色沉淀;
(4)根据苯环上氢原子的种类决定了一溴代物的种类来解答.
解答:解:(1)X元素的质量分数为40.6%,则碳、氢元素的质量分数之和为59.4%,而分子中碳、氢元素的质量比为12:1,求出碳、氢元素的质量分数分别为:59.4%×
=54.8%,59.4%×
=4.6%,又因卤代烃RX2相对分子质量为175,所以一个卤代烃RX2的分子中含有碳原子的个数为
=8,含有氢原子的个数为
=8,而12×8+1×8+M(X)×2=175,所以M(X)=35.5,所以X为Cl,所以分子式为:C8H8Cl2,故答案为:C8H8Cl2;
(2)①根据M、P发生缩聚反应可知,M为E二元醇,N为二元酸,所以M→N→P是醇连续两次氧化生成酸,N为二元醛,含有两个醛基,故答案为:氧化反应;醛基;
②因C8H8Cl2是卤代烃,而卤代烃在碱性条件下发生水解反应生成醇,故答案为:NaOH溶液;
③因C8H8Cl2是卤代烃,结合M、P发生缩聚反应的产物的结构,所以M、P的结构简式分别为: 、
、 ,所以反应Ⅱ的化学方程式为:
,所以反应Ⅱ的化学方程式为: ,
,
故答案为: ;
;
(3)因卤代烃在碱性条件下发生水解反应生成氯化氢,氯化氢能与硝酸银溶液反应生成白色沉淀,所以取少量卤代烃置于试管中,加入1mL5%的NaOH溶液,充分振荡、静置,待溶液分层后取上层水溶液,加入另一只盛有10mL稀硝酸溶液的试管中,然后加入2-3滴2%的硝酸银溶液,有白色沉淀生成,故答案为:取少量卤代烃置于试管中,加入1mL5%的NaOH溶液,充分振荡、静置,待溶液分层后取上层水溶液,加入另一只盛有10mL稀硝酸溶液的试管中,然后加入2-3滴2%的硝酸银溶液,有白色沉淀生成;
(4)因苯环上氢原子的种类决定了一溴代物的种类,故答案为: (任选一种).
(任选一种).
| 12 |
| 13 |
| 1 |
| 13 |
| 175×54.8% |
| 12 |
| 175×4.6% |
| 1 |
(2)①根据M、P发生缩聚反应可知,M为E二元醇,N为二元酸,所以M→N→P是醇连续两次氧化生成酸,N为二元醛,含有两个醛基,故答案为:氧化反应;醛基;
②因C8H8Cl2是卤代烃,而卤代烃在碱性条件下发生水解反应生成醇,故答案为:NaOH溶液;
③因C8H8Cl2是卤代烃,结合M、P发生缩聚反应的产物的结构,所以M、P的结构简式分别为:
 、
、 ,所以反应Ⅱ的化学方程式为:
,所以反应Ⅱ的化学方程式为: ,
,故答案为:
 ;
;(3)因卤代烃在碱性条件下发生水解反应生成氯化氢,氯化氢能与硝酸银溶液反应生成白色沉淀,所以取少量卤代烃置于试管中,加入1mL5%的NaOH溶液,充分振荡、静置,待溶液分层后取上层水溶液,加入另一只盛有10mL稀硝酸溶液的试管中,然后加入2-3滴2%的硝酸银溶液,有白色沉淀生成,故答案为:取少量卤代烃置于试管中,加入1mL5%的NaOH溶液,充分振荡、静置,待溶液分层后取上层水溶液,加入另一只盛有10mL稀硝酸溶液的试管中,然后加入2-3滴2%的硝酸银溶液,有白色沉淀生成;
(4)因苯环上氢原子的种类决定了一溴代物的种类,故答案为:
 (任选一种).
(任选一种).点评:本题主要考查了有机物分子式的确定及有机合成,综合性较强,在确定一溴代物的种类时应根据氢原子的种类来决定,难度不大.

练习册系列答案
相关题目
