0 20911 20919 20925 20929 20935 20937 20941 20947 20949 20955 20961 20965 20967 20971 20977 20979 20985 20989 20991 20995 20997 21001 21003 21005 21006 21007 21009 21010 21011 21013 21015 21019 21021 21025 21027 21031 21037 21039 21045 21049 21051 21055 21061 21067 21069 21075 21079 21081 21087 21091 21097 21105 203614
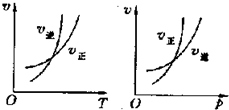 可逆反应mA(g)?nB(g)+pC(s)△H=Q,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( )
可逆反应mA(g)?nB(g)+pC(s)△H=Q,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( ) 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的主要因素是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的主要因素是( )

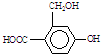 为实现以下物质的转化
为实现以下物质的转化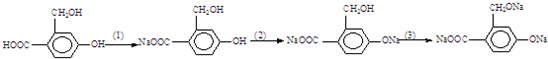
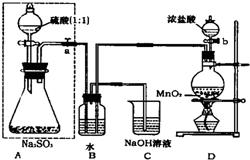 长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来测定亚硫酸钠试剂的被氧化的程度,设计了如图实验:请回答下面的问题:
长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来测定亚硫酸钠试剂的被氧化的程度,设计了如图实验:请回答下面的问题: