0 20529 20537 20543 20547 20553 20555 20559 20565 20567 20573 20579 20583 20585 20589 20595 20597 20603 20607 20609 20613 20615 20619 20621 20623 20624 20625 20627 20628 20629 20631 20633 20637 20639 20643 20645 20649 20655 20657 20663 20667 20669 20673 20679 20685 20687 20693 20697 20699 20705 20709 20715 20723 203614



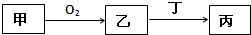 已知甲、乙、丙三种物质均含有同一种短周期元素,其中甲为单质,其转化关系如图,下列说法不正确的( )
已知甲、乙、丙三种物质均含有同一种短周期元素,其中甲为单质,其转化关系如图,下列说法不正确的( )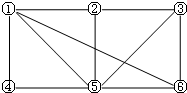 如图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨能还原氧化铁):
如图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨能还原氧化铁):