0 20450 20458 20464 20468 20474 20476 20480 20486 20488 20494 20500 20504 20506 20510 20516 20518 20524 20528 20530 20534 20536 20540 20542 20544 20545 20546 20548 20549 20550 20552 20554 20558 20560 20564 20566 20570 20576 20578 20584 20588 20590 20594 20600 20606 20608 20614 20618 20620 20626 20630 20636 20644 203614
 (1)铅蓄电池的电池总反应式为:
(1)铅蓄电池的电池总反应式为: (1)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
(1)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式: 在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应: O2↑+2H2O
O2↑+2H2O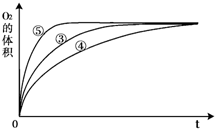


 下列化合物:①HCl ②NaOH ③CH3COOH ④NH3?H2O ⑤CH3COONa ⑥NH4Cl
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3?H2O ⑤CH3COONa ⑥NH4Cl