0 20129 20137 20143 20147 20153 20155 20159 20165 20167 20173 20179 20183 20185 20189 20195 20197 20203 20207 20209 20213 20215 20219 20221 20223 20224 20225 20227 20228 20229 20231 20233 20237 20239 20243 20245 20249 20255 20257 20263 20267 20269 20273 20279 20285 20287 20293 20297 20299 20305 20309 20315 20323 203614
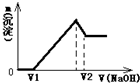 将0.1mol镁、铝合金溶于100mL2mol/L的H2SO4溶液中,然后滴加1mol/L的NaOH溶液,生成沉淀与所加NaOH溶液体积的关系如图所示.试回答下列问题:
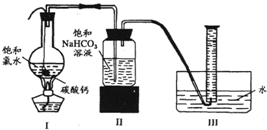
将0.1mol镁、铝合金溶于100mL2mol/L的H2SO4溶液中,然后滴加1mol/L的NaOH溶液,生成沉淀与所加NaOH溶液体积的关系如图所示.试回答下列问题: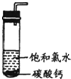 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.2005年的《化学教育》报道了如下实验研究:
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.2005年的《化学教育》报道了如下实验研究: HCl+HClO平衡向右移动,HClO浓度增大
HCl+HClO平衡向右移动,HClO浓度增大