0 19978 19986 19992 19996 20002 20004 20008 20014 20016 20022 20028 20032 20034 20038 20044 20046 20052 20056 20058 20062 20064 20068 20070 20072 20073 20074 20076 20077 20078 20080 20082 20086 20088 20092 20094 20098 20104 20106 20112 20116 20118 20122 20128 20134 20136 20142 20146 20148 20154 20158 20164 20172 203614
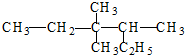 的名称为
的名称为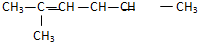 的名称为
的名称为 的分子式为
的分子式为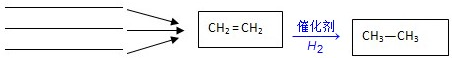

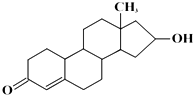 “诺龙”属于国际奥委会明确规定的违禁药品中 合成代谢类的类固醇,其结构简式如图,下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中 合成代谢类的类固醇,其结构简式如图,下列关于“诺龙”的说法中不正确的是( )