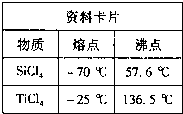
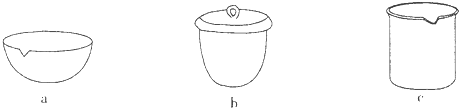
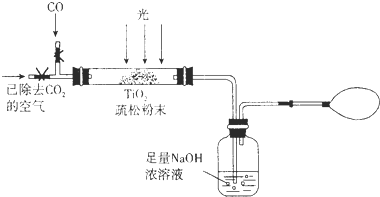
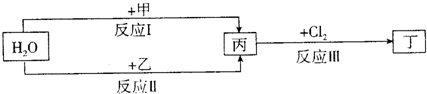
0 19950 19958 19964 19968 19974 19976 19980 19986 19988 19994 20000 20004 20006 20010 20016 20018 20024 20028 20030 20034 20036 20040 20042 20044 20045 20046 20048 20049 20050 20052 20054 20058 20060 20064 20066 20070 20076 20078 20084 20088 20090 20094 20100 20106 20108 20114 20118 20120 20126 20130 20136 20144 203614