0 19356 19364 19370 19374 19380 19382 19386 19392 19394 19400 19406 19410 19412 19416 19422 19424 19430 19434 19436 19440 19442 19446 19448 19450 19451 19452 19454 19455 19456 19458 19460 19464 19466 19470 19472 19476 19482 19484 19490 19494 19496 19500 19506 19512 19514 19520 19524 19526 19532 19536 19542 19550 203614
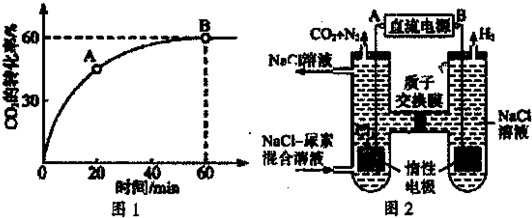
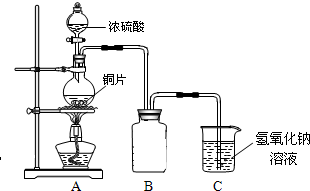 (2011?绵阳模拟)某化学兴趣小组为探究
(2011?绵阳模拟)某化学兴趣小组为探究