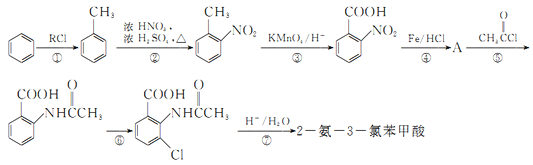
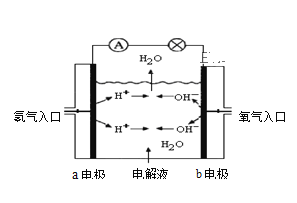
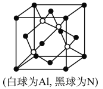
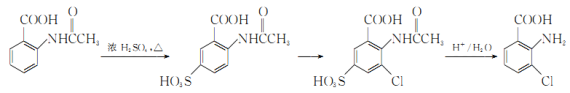0 193919 193927 193933 193937 193943 193945 193949 193955 193957 193963 193969 193973 193975 193979 193985 193987 193993 193997 193999 194003 194005 194009 194011 194013 194014 194015 194017 194018 194019 194021 194023 194027 194029 194033 194035 194039 194045 194047 194053 194057 194059 194063 194069 194075 194077 194083 194087 194089 194095 194099 194105 194113 203614