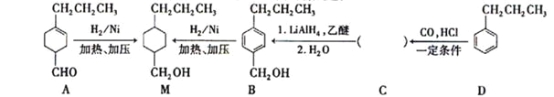
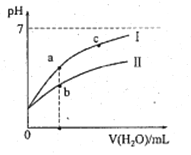
【题目】下表为25℃时某些弱酸的电离平衡常数;下边图像表示25℃时,稀释CH3COOH、HClO两种酸的稀溶液,溶液pH随加水量的变化。常温下,有关说法正确的是
弱酸的电离平衡常数(25℃) | |
CH3COOH | HClO |
Ka=1.8×10-5 | Ka=3.0×10-8 |
A. 图像中,a点酸的总浓度>b点酸的总浓度
B. 图像中,c(H+):c(R-)的值:a点>c点(HR代表CH3COOH或HClO)
C. pH相同的CH3COONa溶液和NaClO溶液的浓度关系:c(CH3COOHNa)<c(NaClO)
D. 两溶液浓度相等,CH3COONa溶液的c(OH-)+c(CH3COO-)>NaClO溶液的c(OH-)+c(C1O-)
【题目】冬青油又叫水杨酸甲酯,是一种重要的有机合成原料。某化学小组用水杨酸(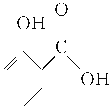 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
实验步骤:
Ⅰ.如图,在三颈烧瓶中加入13.8 g(0.1 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成共沸物,沸点为85 ℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95 ℃下恒温加热反应1.5小时;
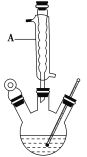
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5% NaHCO3溶液和水洗涤;分离出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221~224 ℃的馏分,得水杨酸甲酯9.12 g。
常用物理常数:
名称 | 分子量 | 颜色状态 | 相对密度 (g·cm-3) | 熔点 (℃) | 沸点 (℃) |
水杨酸 甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 218~ 224 |
水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
请根据以上信息回答下列问题:
(1)仪器A的名称是________,加入沸石的作用是_____________________。若加热后发现未加沸石,应采取的正确方法是________________________________________________。
(2)制备水杨酸甲酯时,最合适的加热方法是____________________________________________。
(3)实验中加入甲苯对合成水杨酸甲酯的作用是___________________________________________。
(4)反应结束后,分离出甲醇采用的方法是__________________________________________。
(5)实验中加入无水硫酸镁的作用是__________________________________________。本实验的产率为________(保留两位有效数字)。