0 19202 19210 19216 19220 19226 19228 19232 19238 19240 19246 19252 19256 19258 19262 19268 19270 19276 19280 19282 19286 19288 19292 19294 19296 19297 19298 19300 19301 19302 19304 19306 19310 19312 19316 19318 19322 19328 19330 19336 19340 19342 19346 19352 19358 19360 19366 19370 19372 19378 19382 19388 19396 203614
 科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( )
科学家最近在-100℃的低温下合成了一种烃X,经红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型.下列说法中错误的是( ) 某同学用碳棒、纯铜片、直流电源和稀硫酸为原材料,实现了在通常条件下不能发生的反应:
某同学用碳棒、纯铜片、直流电源和稀硫酸为原材料,实现了在通常条件下不能发生的反应: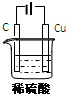
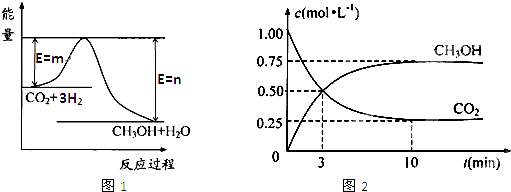
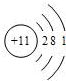
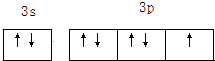
 盖斯定律指出:化学反应的焓变只与各反应物的始态和各生成物的终态有关,而与具体的反应途径无关.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是( )
盖斯定律指出:化学反应的焓变只与各反应物的始态和各生成物的终态有关,而与具体的反应途径无关.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是( )