 (2013?安徽)一定条件下,通过下列反应可以制备特种陶瓷的原料MgO: (2013?安徽)一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2(g)△H>0 该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
|
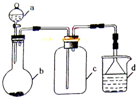 (2013?安徽)实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( ) (2013?安徽)实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
|
 (2013?安徽)一定条件下,通过下列反应可以制备特种陶瓷的原料MgO: (2013?安徽)一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2(g)△H>0 该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
|
 (2013?安徽)实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( ) (2013?安徽)实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
|