0 18718 18726 18732 18736 18742 18744 18748 18754 18756 18762 18768 18772 18774 18778 18784 18786 18792 18796 18798 18802 18804 18808 18810 18812 18813 18814 18816 18817 18818 18820 18822 18826 18828 18832 18834 18838 18844 18846 18852 18856 18858 18862 18868 18874 18876 18882 18886 18888 18894 18898 18904 18912 203614
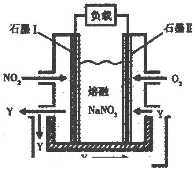

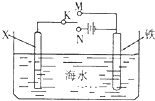 (2011?南京三模)如图是模拟电化学反应装置图.下列说法正确的是( )
(2011?南京三模)如图是模拟电化学反应装置图.下列说法正确的是( )