【题目】现有A~I 9种短周期元素,它们在元素周期表中的位置如下.请据此回答下列问题:
A | ||||||||
D | E | I | ||||||
B | C | F | H | G | ||||
(1)下列中的元素的原子间反应最容易形成离子键的是
A.C和F
B.B和G
C.D和G
D.B和E
(2)下列由A~G形成的各分子中所有原子都满足最外层为8电子结构的是 .
A.EA3
B.AG
C.FG5
D.DG4
(3)由A,E组成的一种化合物化学式为EA5 , 其各原子均达到同周期稀有气体原子的稳定结构,试写出该化合物的电子式 .
(4)B,C,H,G形成的简单离子半径由大到小
(5)A与I形成1:1的化合物的结构式为
(6)写出B的最高价氧化物的水化物与G的最高价氧化物的水化物反应方程式:
写出HI2使酸性高锰酸钾褪色的离子方程式: .
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是__________________________。
(2)利用实验1中的数据,计算用KMnO4表示的化学反应速率为_____________。(溶液混合前后体积变化可忽略)
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
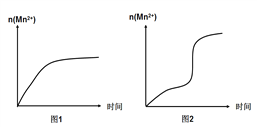
①该小组同学提出的假设是_____________。
②请你帮助该小组同学完成实验方案,并填写表中空白
实验编号 | 室温下,试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | |||
4 | _____________ | 2.0 | 2.0 | 3.0 | MnSO4 | t |
③若该小组同学提出的假设成立,t_____________1.5(填“大于”、“小于”或“等于”)。