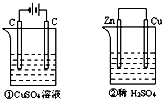
 如图所示的两个装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,则下列叙述正确的是( )
如图所示的两个装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,则下列叙述正确的是( ) 如图所示的两个装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,则下列叙述正确的是( )
如图所示的两个装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,则下列叙述正确的是( ) 如图所示的两个装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,则下列叙述正确的是( )
如图所示的两个装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,则下列叙述正确的是( )