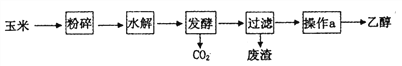
【题目】电离平衡是溶液化学中的重要内容,某化学兴趣小组拟以乙酸为例探究弱酸的性质。
(1)实验一:氢氧化钠标准溶液的配制。
现要配制0.1000mol/LNaOH标准溶液250mL,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管和______,操作过程中如果没有将烧杯等的洗涤液一并转入容量瓶,在其它操作都正确的情况下,将该标准溶液用来滴定下列(2)中的未知浓度的乙酸溶液,将会使侧定的结果偏_(填“高”、“低”、“不影响”)
(2)实验二:现有一瓶乙酸溶液,常温下测定其中乙酸的电离平衡常数。设计实验方案,将待测物理量和对应的测定方法填写在下表中。
待测物理量 | 测定方法 |
①_______ | 量取25.00mL乙酸溶液于锥形瓶中,滴加指示剂,将0.1000mol/LNaOH标准溶液装入碱式滴定管,滴定至终点,记录数据。重复滴定2次。 |
②H+的物质的量浓度 | 取适最乙酸溶液于烧杯中,用______测定溶液pH。 |
③ 上述实验中,如果在某温度时测得乙酸溶液的物质的量浓度为0.1000mol/L,pH=3,则在该温度时乙酸的电离平衡常数为____________。
(3)实验三:探究酸的强弱对酸与镁条反应速率的影响。
① 设计实验方案如下表,表中c=_______g。
编号 | 酸的种类 | 酸的浓度(mol/L) | 酸的体积/mL | 镁条质量/g |
l | 乙酸 | 0.5 | 17.0 | 2.0 |
2 | 盐酸 | 0.5 | 17.0 | c |
② 实验步骤:
a)下图的装置中,在添加药品之前必须________;
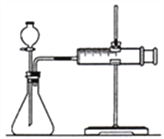
b)反应开始后,__________;
c)将所记录的欲据绘制成曲线图(下图)。

③ 写出镁与乙酸溶液反应的离子方程式:_______________。
④ 描述O~5min盐酸与镁条反应的反应速率变化规律:_____________。