【题目】[化学—选修3:物质结构与性质]
硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4。回答下列问题:
⑴写出基态Zn原子的价电子排布式__________,基态S原子核外未成对电子数为_____。
⑵ZnSO4中三种元素的电负性由大到小的顺序为_____________________,SO42-的立体构型为________________,其中S的杂化轨道类型为_________。
⑶硫酸锌溶于氨水可生成[Zn(NH3)4]SO4溶液,[Zn(NH3)4]SO4溶液中不存在的微粒间作用力有___________。
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
⑷根据下列锌卤化物的熔点和溶解性,判断ZnF2晶体的类型为___________;分析ZnCl2、ZnBr2、ZnI2熔点依次增大的原因________________。
ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
熔点/℃ | 872 | 275 | 394 | 446 |
在乙醇、乙醚中溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
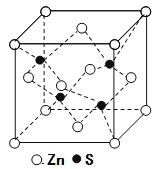
⑸立方ZnS晶体的密度为ρg·cm-3,其晶胞结构如图。S2-周围等距离且最近的Zn2+、S2-依次为______、______;ZnS晶胞中的晶胞参数a=________nm(列出计算式)。
【题目】汽车尾气中的主要污染物是NO、NO2和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
[研究一]用NaOH溶液吸收NO、NO2,
⑴当n(NO)﹕n(NO2)=1时只生成一种盐,这种盐的化学式为__________
⑵当只有NO2时,生成两种盐:2NO2+2NaOH=NaNO2+NaNO3+H2O。若NaOH溶液恰好完全吸收NO2后溶液显碱性,该溶液中离子浓度由大到小的顺序是:___________。
[研究二]一定条件将CO和NO转化为无污染产物:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H
2CO2(g)+N2(g) △H
⑶已知:2C(s)+O2(g)=2CO(g);△H1=-221.0KJ/mol
C(s)+O2(g)=CO2(g);△H2=-393.5KJ/mol
N2(g)+O2(g)=2NO(g);△H3=+180.5KJ/mol。
则△H=______
⑷T℃下,在固定容积的密闭容器中,通入一定量NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) 104 mol/L | 10.0 | 4.50 | 2.00 | 1.50 | 1.00 | 1.00 |
c(CO) 103 mol/L | 3.60 | 3.05 | 2.80 | 2.75 | 2.70 | 2.70 |
①该条件下,2s内N2的平均反应速率v(N2)=_____________
②若往容器中加入一定量生石灰,CO平衡转化率_____(选填“增大”、“减小”或“不变”)
③其它条件不变,只适当升高温度,则4s时,c(NO)=c1mol/L,则c1可能是_______
a.1.10×10﹣3 b.1.25×10﹣4 c.1.00×10﹣4 d.9.00×10﹣5
【研究三】测定汽车尾气中CO的含量
⑸用CO分析仪测定:该分析仪的工作原理类似于燃料电池,其中电解质是能传导O2﹣的Y2O3和ZrO2晶体,负极的电极反应式为____________。
⑹用五氧化二碘(I2O5)固体氧化定量检测:I2O5+5CO=I2+5CO2
抽取10L汽车尾气,用足量I2O5吸收,然后配成100mL溶液,量取其中的20.00mL溶液,用0.0050mol/LNa2S2O3溶液滴定,三次平行实验平均消耗Na2S2O3溶液的体积为20.0mL,已知:2Na2S2O3+I2=Na2S4O6+2NaI,则尾气中c(CO)=___________