0 17684 17692 17698 17702 17708 17710 17714 17720 17722 17728 17734 17738 17740 17744 17750 17752 17758 17762 17764 17768 17770 17774 17776 17778 17779 17780 17782 17783 17784 17786 17788 17792 17794 17798 17800 17804 17810 17812 17818 17822 17824 17828 17834 17840 17842 17848 17852 17854 17860 17864 17870 17878 203614
 某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验.
某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验. 试剂:a.NaOH溶液 b.品红溶液 c.酸性KMnO4溶液 d.Ca(OH)2溶液
试剂:a.NaOH溶液 b.品红溶液 c.酸性KMnO4溶液 d.Ca(OH)2溶液
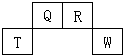 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等,请回答下列问题:

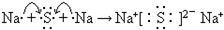


 如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )