8. CO2和CO是工业排放的对环境产生影响的废气.
CO2和CO是工业排放的对环境产生影响的废气.
(1)以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=a kJ•mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);△H=-86.98kJ•mol-1
则a为+72.49kJ.mol-1.
(2)科学家们提出用工业废气中的CO2制取甲醇:CO2+3H2CH3OH+H2O.
制得的CH3OH可用作燃料电池的燃料.
①在KOH介质中,负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②作介质的KOH可以用电解K2SO4溶液的方法制得.则KOH在D出口得到,阳极的电极反应式是:4OH-+4e-=2H2O+O2↑
(3)利用CO与H2反应可合成CH3OCH3.
已知:3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g),△H=-247kJ/mol
在一定条件下的密闭容器中,该反应达到平衡,要提高CO的转化率,可以采取的措施是AE.
A.低温高压 B.加入催化剂 C.体积不变充入氦气D.增加CO的浓度 E.分离出二甲醚
(4)CH3OCH3也可由CH3OH合成.
已知反应2CH3OH(g)=CH3OCH3(g)+H2O(g),在某温度下,在1L密闭容器中加入CH3OH,反应到10分钟时达到平衡,此时测得各组分的浓度如表:
①0-10min内反应速率v(CH3OH)=0.04mol•L-1•min-1.
②该温度下的平衡常数为400.
③若平衡后,再向容器中再加入0.01mol CH3OH和0.2mol CH3OCH3,此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
 CO2和CO是工业排放的对环境产生影响的废气.
CO2和CO是工业排放的对环境产生影响的废气.(1)以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=a kJ•mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);△H=-86.98kJ•mol-1
则a为+72.49kJ.mol-1.
(2)科学家们提出用工业废气中的CO2制取甲醇:CO2+3H2CH3OH+H2O.
制得的CH3OH可用作燃料电池的燃料.
①在KOH介质中,负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
②作介质的KOH可以用电解K2SO4溶液的方法制得.则KOH在D出口得到,阳极的电极反应式是:4OH-+4e-=2H2O+O2↑
(3)利用CO与H2反应可合成CH3OCH3.
已知:3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g),△H=-247kJ/mol
在一定条件下的密闭容器中,该反应达到平衡,要提高CO的转化率,可以采取的措施是AE.
A.低温高压 B.加入催化剂 C.体积不变充入氦气D.增加CO的浓度 E.分离出二甲醚
(4)CH3OCH3也可由CH3OH合成.
已知反应2CH3OH(g)=CH3OCH3(g)+H2O(g),在某温度下,在1L密闭容器中加入CH3OH,反应到10分钟时达到平衡,此时测得各组分的浓度如表:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.01 | 0.2 | 0.2 |
②该温度下的平衡常数为400.
③若平衡后,再向容器中再加入0.01mol CH3OH和0.2mol CH3OCH3,此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
6.在T℃时,向1L固定体积的密闭容器M中加入2mol X和1mol Y,发生如下反应:2X(g)+Y(g)?aZ(g)+W(g)△H=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小.
请回答下列问题:
(1)化学计量数a的值为1.
(2)下列能说明该反应达到了化学平衡状态的是ac(填序号).
a.容器内气体的压强一定b.容器内气体的密度一定
c.容器内Z的分子数一定d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是Q1kJ.若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为QkJ.
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则N(填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M>N(填“>”、“<”或“=”).
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
若在某温度下,2mol X和1mol Y在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为350℃.
请回答下列问题:
(1)化学计量数a的值为1.
(2)下列能说明该反应达到了化学平衡状态的是ac(填序号).
a.容器内气体的压强一定b.容器内气体的密度一定
c.容器内Z的分子数一定d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2mol X、1mol Y和1mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是Q1kJ.若起始时向容器M中加入4mol X和6mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为QkJ.
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2mol X和1mol Y,发生题给反应并达到平衡,则N(填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M>N(填“>”、“<”或“=”).
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
5.总压强为30Mpa时,氮气﹑氢气混合气体(体积比为1:3)通入合成塔,反应达平衡时,压强降为25Mpa则平衡时混合气体中氨气的体积分数为( )
| A. | 25% | B. | 20% | C. | 35% | D. | 30% |
4.在密闭容器中进行反应N2(g)+3H2(g)?2NH3(g);△H=-akJ/mol.N2、H2起始的物质的量分别为10mol和30mol,达到平衡时H2的转化率为25%.并放出热量bkJ若从NH3开始在相同条件下欲使平衡时各成分的百分含量与前者相同,则其NH3的转化率和吸收的热量为( )
| A. | 25%和7.5akJ | B. | 25%和3bkJ | C. | 75%和(a-b) kJ | D. | 75%和(10a-b) kJ |
3.某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,其他条件不变时,若改变影响平衡的一个条件,测得容器中物质的浓度、反应速率随时间的变化如图所示.下列说法中正确是:( )


| A. | 30min时降低温度,40min时升高温度 | |
| B. | 前8min A的平均反应速率为0.17mol/(L•min) | |
| C. | 反应方程式中的x=1,正反应为吸热反应 | |
| D. | 20min~40min间该反应的平衡常数均为4 |
2. 硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
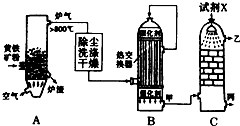
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称).
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂且有热交换器的接触室(填设备名称)中进行反应.在如图所示的装置中,C处流出的气体有SO3、SO2、O2;SO3进入吸收塔(填设备名称)用98.3%的H2SO4吸收,得到浓硫酸或发烟硫酸.
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是400℃,1个标准大气压.
(4)吸收塔排出的尾气中SO2的含量如果超过500μL/L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式2NH3•H2O+SO2=(NH4)2SO3+H2O.
 硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,该反应在沸腾炉中进行(填设备名称).
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂且有热交换器的接触室(填设备名称)中进行反应.在如图所示的装置中,C处流出的气体有SO3、SO2、O2;SO3进入吸收塔(填设备名称)用98.3%的H2SO4吸收,得到浓硫酸或发烟硫酸.
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是400℃,1个标准大气压.
| 压强/MPa SO2转化率 温度/℃ | 1个大气压 | 5个大气压 | 10个大气压 | 15个大气压 |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9989 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8528 | 0.8897 | 0.9276 | 0.9468 |
5.在一密闭容器中有HCHO、H2、和O2混合气体共10g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重4g,则原混合气体中O2的质量分数是( )
| A. | 40% | B. | 33.3% | C. | 60% | D. | 36% |
4.下列有机物中不属于醇类的是( )
0 173933 173941 173947 173951 173957 173959 173963 173969 173971 173977 173983 173987 173989 173993 173999 174001 174007 174011 174013 174017 174019 174023 174025 174027 174028 174029 174031 174032 174033 174035 174037 174041 174043 174047 174049 174053 174059 174061 174067 174071 174073 174077 174083 174089 174091 174097 174101 174103 174109 174113 174119 174127 203614
| A. | 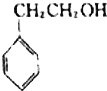 | B. | 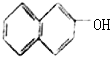 | C. | 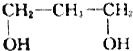 | D. | 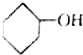 |
 合成氨工业、硝酸工业、硫酸工业是化学工业的重要组成部分.请回答下列问题:
合成氨工业、硝酸工业、硫酸工业是化学工业的重要组成部分.请回答下列问题: