1.T℃时,将3molX和4molY充入1L密闭容器中,发生反应X(g)+3Y(g)?Z(g)+W(g),溶液中Y的物质的量浓度随时间变化如图中实线I所示,图中Ⅱ、Ⅲ表示仅改变某一反应条件时,Y的物质的量浓度随时间的变化,下列说法正确的是( )

| A. | 反应开始至a点时,v(X)=1mol•L-1•min-1 | |
| B. | 4min时,正反应速率:Ⅱ>Ⅰ | |
| C. | 曲线Ⅲ对应点的条件改变是减小压强 | |
| D. | T℃时,该反应的化学平衡常数为1 |
20.下列有关离子检验的叙述正确的是( )
| A. | 向某溶液中加入盐酸化的BaCl 2 溶液,产生白色沉淀,说明溶液中含有SO${\;}_{4}^{2-}$ | |
| B. | 向溶液中通入CO2气体产生的白色沉淀,说明溶液中含有Ca2+ | |
| C. | 含有大量Cl-、CO${\;}_{4}^{2-}$、OH-的五色溶液中,可以依次加入酚酞、BaCl2、硝酸酸化的AgNO3溶液加以验证 | |
| D. | 向某浅绿色溶液中加入KSCN溶液后溶液不变红,再加入H2O2溶液后溶液变红,说明其中含有Fe2+ |
19.常温下,将0.1mol•L-1的一元酸HCl和BOH溶液等体积混合,测得混合液的pH=5,下列判断正确的是( )
| A. | 等浓度的两溶液中水的电离程度:HCl>BOH | |
| B. | BOH的电离方程式是BOH?B++OH- | |
| C. | 混合溶液中:c(B)+>c(OH-)>c(Cl-)>c(H)+ | |
| D. | 要使混合溶液的pH=7,则需VHCl>VBOH |
18.室温时在下列溶液中.可能大量共存的一组离子( )
| A. | pH=1的溶液中:NH${\;}_{4}^{+}$、Fe3+、SO${\;}_{4}^{2-}$、I- | |
| B. | 通入SO2气体产生白色沉淀的溶液中:Fe2+、N0${\;}_{3}^{-}$、Ba2+、H+ | |
| C. | c(HCO${\;}_{3}^{-}$)=0.1 mol/L的溶液中:Al3+、Na+、AlO${\;}_{2}^{-}$、SO${\;}_{4}^{2-}$ | |
| D. | 由水电离出的c(H)+=1×10-13mol/L的溶液中:Na+、S042-、Cl-、K+ |
17. X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电于数是内层
X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电于数是内层
电子数的3倍,下列说法中不正确的是( )
 X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电于数是内层
X、Y、Z、W均为短周期元素,在周期表中位置如图所示.Y原子的最外层电于数是内层电子数的3倍,下列说法中不正确的是( )
| A. | 气态氢化物的稳定性:Y>Z | |
| B. | 最高价氧化物物对应水化物酸性:Z>W | |
| C. | X的气态氢化物与Y、Z、W的气态氢化物都可以反应 | |
| D. | 气态氢化物的沸点,Y最高 |
16.下列有关材料的叙述不正确的是( )
0 173901 173909 173915 173919 173925 173927 173931 173937 173939 173945 173951 173955 173957 173961 173967 173969 173975 173979 173981 173985 173987 173991 173993 173995 173996 173997 173999 174000 174001 174003 174005 174009 174011 174015 174017 174021 174027 174029 174035 174039 174041 174045 174051 174057 174059 174065 174069 174071 174077 174081 174087 174095 203614
| A. | 水晶、陶瓷、玻璃的主要成分都是硅酸盐 | |
| B. | 合金的熔点通常比組分金属低.硬度比组合分金属高 | |
| C. | 自行车钢架生锈主要是电化学腐蚀所致 | |
| D. | 聚氯乙烯不能做食品包装袋 |
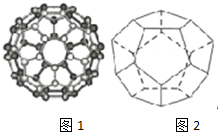 碳是最早被发现和利用的元素之一,长期以来人们以为单质碳的同素异形体只有精钢石、石墨、和无定型碳三种,1985年C60的发现将人类领入认识碳的全新领域--富勒烯,美国科学家Curl和Stnalley教授及英国科学家Kicto教授为此获得了1996年闹贝尔化学奖
碳是最早被发现和利用的元素之一,长期以来人们以为单质碳的同素异形体只有精钢石、石墨、和无定型碳三种,1985年C60的发现将人类领入认识碳的全新领域--富勒烯,美国科学家Curl和Stnalley教授及英国科学家Kicto教授为此获得了1996年闹贝尔化学奖 取一定浓度的NaOH溶液,通入一定量的CO2气体后,再逐滴加入0.1mol/L的盐酸,产生的CO2气体体积(标准状况)与所加入盐酸的体积之间的关系如图所示,
取一定浓度的NaOH溶液,通入一定量的CO2气体后,再逐滴加入0.1mol/L的盐酸,产生的CO2气体体积(标准状况)与所加入盐酸的体积之间的关系如图所示, A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示,试写出符合下列条件的化学方程式:
A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示,试写出符合下列条件的化学方程式: