12.下列离子方程式书写正确的是( )
| A. | FeCl3溶液与单质铜反应:2Fe3++3Cu═2Fe+3Cu2+ | |
| B. | Ba(OH)2溶液与盐酸反应:H++OH-═H2O | |
| C. | AlCl3溶液加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | Na2O与水混合生成烧碱:O2-+H2O═2OH- |
10. X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )
X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )
 X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )
X气体为SO2和CO2的混合气体,Y气体为Cl2,它们同时通入盛有足量氯化钡溶液的洗气瓶中(如下图所示装置).下列说法正确的是( )| A. | 洗气瓶中产生的沉淀是亚硫酸钡 | B. | 洗气瓶中产生的沉淀是碳酸钡 | ||
| C. | 洗气瓶中没有明显现象 | D. | 洗气瓶中有硫酸钡沉淀 |
8.已知2H2O2(aq)=2H2O(l)+O2(g)△H=-196KJ•mol-1,常温下,往H2O2溶液中滴加少量FeCl2溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列有关反应的说法正确的是( )
| A. | 在H2O2分解过程中,溶液的pH逐渐下降 | |
| B. | Fe3+是该反应的催化剂 | |
| C. | 2H2O(l)+O2(g)=2H2O2(aq)在一定条件下能够自发进行 | |
| D. | v(H2O2)=2v(O2) |
7.为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是( )
| 选项 | 实验目的 | 主要玻璃仪器 | 试剂 |
| A | 分离乙醇和乙酸混合物 | 蒸馏烧瓶、冷凝管、酒精灯、温度计、锥形瓶 | 乙醇和乙酸混合物 |
| B | 鉴别NH4Cl中的阳离子 | 试管、酒精灯 | NH4Cl、红色石蕊试纸、蒸馏水 |
| C | 实验室制取CO2 | 试管、带导管的橡皮塞 | 大理石、稀H2SO4 |
| D | 测定FeSO4溶液浓度 | 滴定管、锥形瓶、烧杯 | FeSO4溶液、0.1000mol•L-1KMnO4 |
| A. | A | B. | B | C. | C | D. | D |
6.将铜片溶于稀硝酸中,发生下列反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O在上述反应中,未被还原的HNO3和被还原HNO3的个数比为( )
| A. | 3:1 | B. | 1:3 | C. | 2:3 | D. | 3:2 |
4.氯化铵是一种重要化工原料,也是一种常用的氨肥.
(1)氯化铵作为化肥时不宜与草木灰(主要成分K2CO3)混用.其原因是氯化铵与碳酸钾发生相互促进的水解反应生成氨气,会降低肥效.
(2)热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:6NH4++Fe2O3$\frac{\underline{\;加热\;}}{\;}$2Fe3++6NH3↑+3H2O.
(3)常温下,在20mLamol.L-1氨水中滴加加20mLbmol.L-1HCl溶液恰好至溶液呈中性.计算常温下,NH3.H2O的电离常数Kb=$\frac{a}{a-b}$×10-7mol/L(用含a,b的精确代数式表示)
(4)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
限选药品和仪器:恒温水浴、pH计、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液.
①实验中,“待测物理量”是溶液的pH.
②i=30;ii:探究温度对氯化铵水解平衡的影响.
③上述表格中,y>(填“>”“<”或“=”)m.
(1)氯化铵作为化肥时不宜与草木灰(主要成分K2CO3)混用.其原因是氯化铵与碳酸钾发生相互促进的水解反应生成氨气,会降低肥效.
(2)热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:6NH4++Fe2O3$\frac{\underline{\;加热\;}}{\;}$2Fe3++6NH3↑+3H2O.
(3)常温下,在20mLamol.L-1氨水中滴加加20mLbmol.L-1HCl溶液恰好至溶液呈中性.计算常温下,NH3.H2O的电离常数Kb=$\frac{a}{a-b}$×10-7mol/L(用含a,b的精确代数式表示)
(4)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
| 实验序号 | c(NH4Cl)/mol.L-1 | 温度/℃ | 待测物理量 | 实验目的 |
| Ⅰ | 0.5 | 30 | x | - |
| Ⅱ | 1.5 | i | y | 探究浓度对氯化铵水解平衡的影响 |
| Ⅲ | 0.5 | 35 | z | ii |
| Ⅳ | 2.0 | 40 | m | 探究温度、浓度同时对氯化铵水解平衡的影响 |
①实验中,“待测物理量”是溶液的pH.
②i=30;ii:探究温度对氯化铵水解平衡的影响.
③上述表格中,y>(填“>”“<”或“=”)m.
3.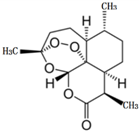 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
0 173852 173860 173866 173870 173876 173878 173882 173888 173890 173896 173902 173906 173908 173912 173918 173920 173926 173930 173932 173936 173938 173942 173944 173946 173947 173948 173950 173951 173952 173954 173956 173960 173962 173966 173968 173972 173978 173980 173986 173990 173992 173996 174002 174008 174010 174016 174020 174022 174028 174032 174038 174046 203614
 2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )
2015年10月,中国女药学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖.这是中国生物医学界迄今为止获得的世界级最高级大奖.青蒿素的键线式化学结构如图所示,下列说法不正确的是( )| A. | 青蒿素属于芳香化合物,能与H2发生加成反应 | |
| B. | 青蒿素能与氢氧化钠溶液发生反应 | |
| C. | 青蒿素的化学式为C15H22O5 | |
| D. | 青蒿素的核磁共振谱图中有12个峰 |
 和一个-Cl.它的可能的结构有4种,写出其中一种的结构简式CH3CH2CH2CHClCH3.
和一个-Cl.它的可能的结构有4种,写出其中一种的结构简式CH3CH2CH2CHClCH3.