9.下列叙述正确的是( )
| A. | SO2具有漂白性,能使碘的淀粉溶液由蓝色变为无色 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 少量金属钠通常保存在煤油中,着火时可用细沙覆盖灭火 | |
| D. | 实验室中用石灰水区分Na2CO3与NaHCO3两瓶无标签溶液 |
6.下列有关说法正确的是( )
| A. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| B. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1 mol•L-1 | |
| C. | Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg | |
| D. | 1molNa2O2固体中含离子总数为3NA |
5.化工生产中原料转化与利用非常重要,现有反应:CCl4+H2?CHCl3+HCl,查阅资料可知沸点:CCl4为77℃,CHCl3为61.2℃.在密闭容器中,该反应达到平衡后,测得下表数据(假设不考虑副反应).
(1)在100℃时,此反应的化学平衡常数表达式为$\frac{c(CHC{l}_{3})×c(HCl)}{c(CC{l}_{4})×c({H}_{2})}$;在110℃时的平衡常数为1.
(2)在实验2中,若1小时后反应达到平衡,则H2的平均反应速率为0.5mol/(L.h),在此平衡体系中再加入0.5molCCl4和1.0molHCl,平衡将向逆 方向移动.(填正、逆或不移动)
(3)实验1中,CCl4的转化率a>50%(填“>”、“=”或“<”).实验3中,b的值D (填字母序号).
A.等于50% B.大于50% C.小于50% D.由本题所给资料无法判断.
| 实验 序号 | 温度℃ | 初始CCl4浓度 (mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1.2 | a |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | b |
(2)在实验2中,若1小时后反应达到平衡,则H2的平均反应速率为0.5mol/(L.h),在此平衡体系中再加入0.5molCCl4和1.0molHCl,平衡将向逆 方向移动.(填正、逆或不移动)
(3)实验1中,CCl4的转化率a>50%(填“>”、“=”或“<”).实验3中,b的值D (填字母序号).
A.等于50% B.大于50% C.小于50% D.由本题所给资料无法判断.
4.在容积为2L的密闭容器中进行反应,CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,n(CH3OH)与反应时间t的变化曲线如图,下列说法正确的是( )


| A. | 该反应的△H<0 | |
| B. | 其他条件不变,升高温度反应的平衡常数增大 | |
| C. | 300℃时,0~t1min内CH3OH的平均生成速率为$\frac{{n}_{1}}{{t}_{1}}$1mol•L-1•min-1 | |
| D. | A点的反应体系温度从300℃升高到500℃,达到平衡时,$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$减小 |
3.反应Fe(固)+CO2(气)?FeO(固)+CO(气)的平衡常数为K1;
反应Fe(固)+H2O(气)?FeO(固)+H2(气)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
(1)推导反应CO2(气)+H2(气)?CO(气)+H2O(气)的平衡常数K与K1、K2的关系式:$\frac{{K}_{1}}{{K}_{2}}$.
(2)计算K值:温度为973开时K=0.618;1173开时:K=1.29.通过K值的计算(1)反应是吸热 反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2,在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
①前2min,用CO表示的该化学反应的速率是:0.0013mol/(L.min).
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原因是升高温度或移走水蒸气.
0 173832 173840 173846 173850 173856 173858 173862 173868 173870 173876 173882 173886 173888 173892 173898 173900 173906 173910 173912 173916 173918 173922 173924 173926 173927 173928 173930 173931 173932 173934 173936 173940 173942 173946 173948 173952 173958 173960 173966 173970 173972 173976 173982 173988 173990 173996 174000 174002 174008 174012 174018 174026 203614
反应Fe(固)+H2O(气)?FeO(固)+H2(气)的平衡常数为K2.
在不同温度时K1、K2的值如下表:
| 温度(绝对温度) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(2)计算K值:温度为973开时K=0.618;1173开时:K=1.29.通过K值的计算(1)反应是吸热 反应(填“吸热”或“放热”).
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2,在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件.各物质的浓度变化如下表:
| 时间/min | CO2 | H2 | CO | H2O |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
②在3~4min之间,反应处于平衡状态(填“平衡”或“非平衡”).
③第6min时,平衡向正反应方向移动,可能的原因是升高温度或移走水蒸气.
 某溶液含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程如图所示:
某溶液含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程如图所示: 其名称是2,4-二甲基-3-乙基-己烷.
其名称是2,4-二甲基-3-乙基-己烷.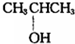 ⑨$\stackrel{13}{6}$C ⑩CH3OH.
⑨$\stackrel{13}{6}$C ⑩CH3OH.